 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算下列甲醇(1)一水(2)系统的组分逸度。 (1)p=101325Pa,T=81.48℃,y1=0.582的气相; (2)p=101325
计算下列甲醇(1)一水(2)系统的组分逸度。 (1)p=101325Pa,T=81.48℃,y1=0.582的气相; (2)p=101325Pa,T=81.48℃,x1=0.2的液相。已知液相符合Wilson方程,其模型参数是
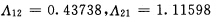 。
。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算下列甲醇(1)一水(2)系统的组分逸度。 (1)p=101325Pa,T=81.48℃,y1=0.582的气相; (2)p=101325Pa,T=81.48℃,x1=0.2的液相。已知液相符合Wilson方程,其模型参数是
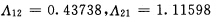 。
。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“计算下列甲醇(1)一水(2)系统的组分逸度。 (1)p=10…”相关的问题
更多“计算下列甲醇(1)一水(2)系统的组分逸度。 (1)p=10…”相关的问题
计算甲醇(1)一水(2)系统的露点(假设气相是理想气体,可用软件计算)。(1)p=101325Pa,y1=0.582(实验值T=81.48℃,x1=0.2);(2)T=67.83℃,y1=0.914(实验值p=101325Pa,x1=0.8)。 已知:Wilson能量参数λ12—λ11=1085.13J/mol和λ21一λ22=1631.04 J/mol。
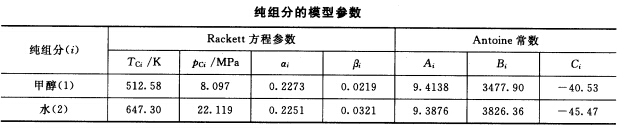
利用Wilsorl方程,计算下列甲醇(1)-水(2)系统的组分逸度(a)p=101325Pa,T=81.48℃,y1=0.582的气相;(b)p=101325Pa,T=81.48℃,x1=0.2的液相。已知液相符合Wilson方程,其模型参数是

A.k与tR增大;
B.k与tR减小;
C.k与tR不变;
D.k增大,tR减小。
测定了异丁醛(1)一水(2)系统在30℃时的液液平衡数据是x1α=0.8931,x1=0.0150。由此计算van Laar常数。已知30℃时,p1s=28.58kPa,p2s=4.22 kPa。
用PR方程计算1.016MPa,273.15K,y1=0.8962的CO2(1)-正丁烷(2)系统的摩尔体积、组分逸度和总逸度。设K12=0.12。
液态氩(1)-甲烷(2)系统的超额Gibbs函数表达式是
T/K | A | B |
109.0112.0115.74 | 0.30360.29440.2804 | -0.01690.01180.0546 |
计算等物质的量混合物的(1)112.0K的两组分的活度系数;(2)混合热;(3)超额熵。
在101.325kPa下连续操作的精馏塔中分离甲醇一水溶液。进料流量为100kmol/h,进料中甲醇的组成为0.3(摩尔分数),馏出液流量为50kmol/h,回流比R=2。甲醇一水气液相平衡数据见教材附录。
3,CB=0.0622kmol/m3,uA=0.0017m/s,uB=0.0003m/s,试计算:
1)u、um;
2)NA、NB、N;
3)mA、mB、m。