 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在100.00 mL含亚砷酸盐的NaHCO3缓冲溶液中,用库仑滴定法电解产生I2来进行滴定,电极反应为 在1
在100.00 mL含亚砷酸盐的NaHCO3缓冲溶液中,用库仑滴定法电解产生I2来进行滴定,电极反应为
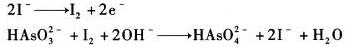 在1.00 mA的恒电流下经316 s达到终点,试计算试液中HASO32-的浓度?
在1.00 mA的恒电流下经316 s达到终点,试计算试液中HASO32-的浓度?
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在100.00 mL含亚砷酸盐的NaHCO3缓冲溶液中,用库仑滴定法电解产生I2来进行滴定,电极反应为
 在1.00 mA的恒电流下经316 s达到终点,试计算试液中HASO32-的浓度?
在1.00 mA的恒电流下经316 s达到终点,试计算试液中HASO32-的浓度?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在100.00 mL含亚砷酸盐的NaHCO3缓冲溶液中,用库…”相关的问题
更多“在100.00 mL含亚砷酸盐的NaHCO3缓冲溶液中,用库…”相关的问题
准确量取30.00 mL弱酸HA,加水稀释至100.00 mL,在电池:(—)SHE|HA || SCE()中,以0.100 0 mol·L-1NaOH标准溶液滴定之。25℃时,当弱酸HA被中和一半时,电池电动势为0.524 V,化学计量点时,电池电动势为0.749 V。求:(1)弱酸HA的电离常数Kα值。(2)原弱酸HA溶液的浓度?(已知饱和甘汞电极的电极电位为0.244 V)
(提示:反应为CH2OHCH2OH+



I2+

在pH=10的氨缓冲溶液中,滴定100.00mL含Ca2+、Mg2+的水样,消耗0.01016mol/L的EDTA标准溶液15.28mL;另取100.00mL水样,用NaOH处理,使Mg2+生成Mg(OH)2沉淀,滴定时消耗EDTA标准溶液10.43mL,计算水样中CaCO3和MgCO3的含量(以mg/L表示)。