 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
根据标准溶液的浓度和所消耗的体积,算出待测组分的含量,这一分析方法称为______。滴加标准溶液的操作过程为_
_____。滴加的标准溶液组分恰好反应完全的一点,称为______。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“根据标准溶液的浓度和所消耗的体积,算出待测组分的含量,这一分…”相关的问题
更多“根据标准溶液的浓度和所消耗的体积,算出待测组分的含量,这一分…”相关的问题
用同一浓度的H2C2O4标准溶液,分别滴定等体积的KMnO4和NaOH两种溶液,化学计量点时如果消耗的标准溶液体积相等,说明NaOH溶液的浓度是KMnO4溶液浓度的5倍。( )
用同一NaOH标准溶液滴定相同浓度的不同一元弱酸时,若弱酸的解离常数 越大,则()。
越大,则()。
A、消耗NaOH标准溶液的体积越大
B、消耗NaOH标准溶液的体积越小
C、滴定突跃范围越大
D、滴定突跃范围越小
A.#图片0$#
B.#图片1$#
C.#图片2$#
D.#图片3$#
用CLa(No3)3=0.03318mol?L-1的La(NO3)3溶液滴定100.0mL 0.03095mol?L-1的NaF的溶液,滴定反应为:
 ,用固体LaF。膜电极为指示电极(正极),饱和甘汞电极为参比电极(负级),测得其滴定数据为:
,用固体LaF。膜电极为指示电极(正极),饱和甘汞电极为参比电极(负级),测得其滴定数据为:
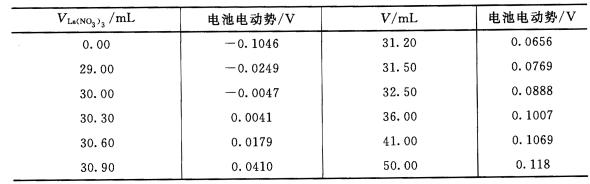 (1)计算反应完全时所需滴定剂的体积,并将其与电位滴定确定终点时消耗滴定剂的体积相比较。 (2)已知电池电动势与F一浓度的关系为:E=K+0.0592PF,用所测第一组数据算出K值。 (3)用求得的K值,计算加入50.00mI.,滴定剂后r的浓度?(设活度系数不变)
(1)计算反应完全时所需滴定剂的体积,并将其与电位滴定确定终点时消耗滴定剂的体积相比较。 (2)已知电池电动势与F一浓度的关系为:E=K+0.0592PF,用所测第一组数据算出K值。 (3)用求得的K值,计算加入50.00mI.,滴定剂后r的浓度?(设活度系数不变)