 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
计算0.10mol/L NaHCO3溶液的pH为多少?
计算0.10mol/L NaHCO3溶液的pH为多少?
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算0.10mol/L NaHCO3溶液的pH为多少?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“计算0.10mol/L NaHCO3溶液的pH为多少?”相关的问题
更多“计算0.10mol/L NaHCO3溶液的pH为多少?”相关的问题
计算pH=5.0时,0.10mol/L H2C2O4溶液中的浓度。(已知:H2C2O4的Ka1=5.9×10-2,Ka2=6.4×10-5)
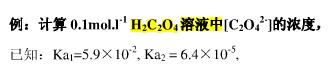
用0.01mol/L EDTA滴定20.00mL0.01mol/L Ni2+,在pH=10的氨缓冲溶液中,使溶液中游离氨的浓度为0.10mol/L。计算lgK'NiY化学计量点时溶液中pNi'和pNi。


已知c(
计算密度为1.05g/mL的冰醋酸(含HAc 99.6%)的物质的量浓度。欲配制0.10mol/L醋酸溶液500mL,应取该冰醋酸多少毫升?已知M(HAc)=60.05g/mol。