 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
某弱酸HA的Ka=1.0×10-4,则其1mol/L水溶液的pH为( )。
A.2.0
B.3.0
C.4.0
D.6.0
E.8.0
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.2.0
B.3.0
C.4.0
D.6.0
E.8.0
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某弱酸HA的Ka=1.0×10-4,则其1mol/L水溶液的…”相关的问题
更多“某弱酸HA的Ka=1.0×10-4,则其1mol/L水溶液的…”相关的问题
A.5×10-10B.
有一弱酸HA,其离解常数Ka=6.4×10-7,计算c(HA)=0.30mol·L-1时溶液的c(H+)。
已知二元弱酸H2B的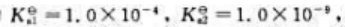 则二元弱碱B的K为().
则二元弱碱B的K为().
A、1.0×10-4
B、1.0×10-9
C、1.0×10-5
D、1.0×10-4
A.1.0×10-4
B.1.0×10-5
C.1.0×10-6
D.1.0×10-7
A.NH2OH(Kb=1×10-9)
B.NH3·H2O(Kb=1×10-5)
C.HAc(Ka=1×10-5)
D.HCOOH(Ka=1×10-4)
E.HNO2(Ka=5×10-4)
A.羟氨(NH2OH)Kb=1×10-9
B.氨水Kb=1×10-5
C.甲酸Ka=1×10-4
D.乙酸Ka=1×10-5