 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
NaOH标准溶液滴定HAc至化学计量点时H+浓度的计算式为()。 A. B. C. D.
NaOH标准溶液滴定HAc至化学计量点时H+浓度的计算式为( )。
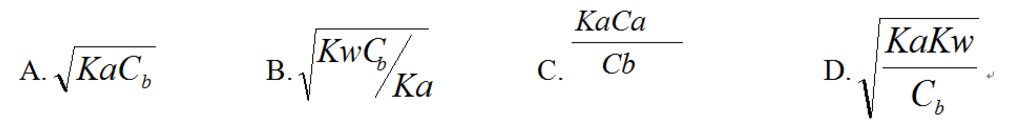
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
NaOH标准溶液滴定HAc至化学计量点时H+浓度的计算式为( )。
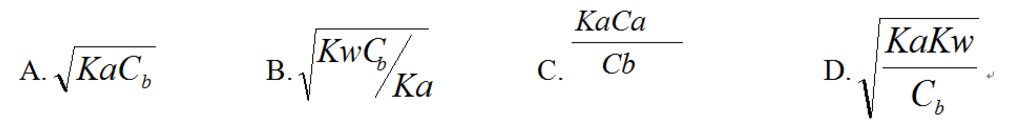
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“NaOH标准溶液滴定HAc至化学计量点时H+浓度的计算式为(…”相关的问题
更多“NaOH标准溶液滴定HAc至化学计量点时H+浓度的计算式为(…”相关的问题
A.偏高
B.偏低
C.无影响
D.无法确定
用同一浓度的H2C2O4标准溶液,分别滴定等体积的KMnO4和NaOH两种溶液,化学计量点时如果消耗的标准溶液体积相等,说明NaOH溶液的浓度是KMnO4溶液浓度的5倍。( )
用0.2000mol·L-1Ba(OH)2溶液滴定0.1000mol·L-1HAc溶液至化学计量点时,溶液的pH值为多少?[Ka(HAc)=1.8×10-5]
A.V1>V2
B.V1=V2
C.V1 < V2
D.无法确定V1和V2的相对大小
以0.01667mol/L K2Cr2O7标准溶液滴定0.1000mol/L的Fe2+至终点时,溶液的pH=2.0,求化学计量点电位。
A.化学计量点前后0.1%的pH均增大
B.化学计量点前0.1%的pH不变,后0.1%的pH增大
C.化学计量点前0.1%的pH减小,后0.1%的pH增大
D.化学计量点前后0.1%的pH均减小
取某一元弱酸(HA)纯品1.250g,溶成50mL水溶液。用NaOH溶液(0.090mol·dm-3)滴定至化学计量点,消耗41.20mL。在滴定过程中,当滴定剂加到8.24mL时,溶液的pH为4.30。计算:
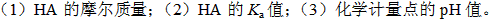
A.偏高
B.偏低
C.无影响
D.不能确定
E.全部不对