 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
计算0.010mol·dm-3的H2SO4溶液中各离子的浓度,已知H2SO4的Kθ2为1.2×10-2⊕
计算0.010mol·dm-3的H2SO4溶液中各离子的浓度,已知H2SO4的Kθ2为1.2×10-2。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算0.010mol·dm-3的H2SO4溶液中各离子的浓度,已知H2SO4的Kθ2为1.2×10-2。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“计算0.010mol·dm-3的H2SO4溶液中各离子的浓度…”相关的问题
更多“计算0.010mol·dm-3的H2SO4溶液中各离子的浓度…”相关的问题
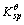 =1.2×10-10,SrCrO4的
=1.2×10-10,SrCrO4的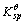 =2.2×10-5。
=2.2×10-5。
已知原电池:
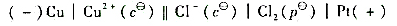
的电动势为 。
。
(1)试求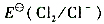 ;
;
(2)若正极Cl2的压力为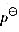 ,Cl-离子的初始浓度为0.10moldm-3,负极Cu2+离子的初始浓度为0.010mol·dm-3,试求原电池的电动势E池。
,Cl-离子的初始浓度为0.10moldm-3,负极Cu2+离子的初始浓度为0.010mol·dm-3,试求原电池的电动势E池。
0.010mol·L-1SrCl2溶液2mL和0.010mol·L-1K2SO4溶液3mL混合,通过计算说明有无沉淀生成。已知SrSO4的Ksp=3.2×10-7。
已知298K时某一元弱酸的浓度为0.010mol·L-1,测得其pH为4.00,计算Ka和α。
已知298K时某一元弱酸的浓度为0.010mol·L-1,测得其pH为4.00,计算Ka和α。
根据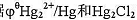 的溶度积计算
的溶度积计算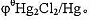 如果溶液中CI浓度为
如果溶液中CI浓度为
0.010mol·L-1,Hg2Cl2/Hg电对的电位为多少?
计算下列溶液的pH:
(1)0.10mol·L-1NaAc溶液;
(2)0.10mol·L-1NH4Cl溶液;
(3)0.010mol·L-1H2SO4溶液;
(4)0.10mol·L-1Na3PO4溶液;
(5)0.10mol·L-1NaH2PO4溶液;