 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
溶液的酸碱性是由氢离子浓度和氢氧根离子浓度所决定的,当氢离子浓度[H£«]大于氢氧根离子浓度[OH£]时,溶液显()性。用PH值可直接反映出溶液酸碱性,PH>7时溶液显()性。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“溶液的酸碱性是由氢离子浓度和氢氧根离子浓度所决定的,当氢离子…”相关的问题
更多“溶液的酸碱性是由氢离子浓度和氢氧根离子浓度所决定的,当氢离子…”相关的问题
A.<3
B.<5
C.<7
D.<9
A.随溶液中氢离子活度的增高向负方向移动;
B.随溶液中氢离子活度的增高向正方向移动;
C.随溶液中氢氧根离子活度的增高向正方向移动;
D.随溶液pH的增高向正方向移动。
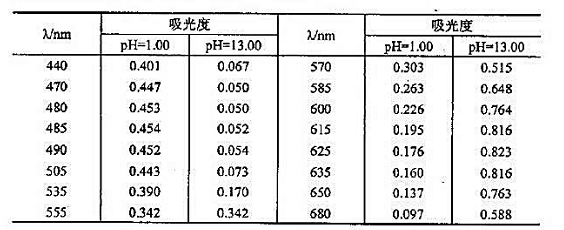
(1)指示剂酸型是什么颜色?在酸性介质中测定时应选什么颜色的滤光片?在强碱性介质中测定时应选什么波长?
(2)绘制指示剂酸式和诚式离子的吸收曲线.
(3)当用2cm比色皿在590nm处测量强碱性介质中指示剂浓度为1.00x10-4mol·L-1溶液时吸光度为多少?
(4)若题设溶液在485nm处,用1cm比色m测得吸光度为0.309.此染液pH为多少?如在555m测定,此溶液吸光度是多少?
(5)在什么波长处测定指示剂的吸光度与pH无关?为什么?
(6)欲用标准曲线法测定指示剂总浓度,需选择什么实验条件才能使标准由线不偏高比尔定律?
A.强酸溶液中的氢离子浓度一定等于该酸的分析浓度
B.弱酸溶液中的氢离子浓度等于该酸的分析浓度
C.弱酸溶液中的氢离子浓度肯定比强酸溶液中的氢离子浓度低
D.弱酸溶液中的氢离子浓度可根据其电离平衡常数计算得到
A.HAc(Ka=1.8×10-5) B.H3BO3(
C.H2C2O4(
E.HCl(Ka
A.HAc(Ka=1.8×10-5) B.H3BO3(
C.H2C2O4(
E.HCl(Ka
将KI溶液加到含有0.20mol/L Pb2+和0.01mol/L Ag+的溶液中,哪种离子先沉淀?第二种离子沉淀时第一种离子的浓度是多少?
完成并配平下列化学反应方程式:
(1)过氧化氢在碱性介质中氧化亚铬酸根离子;
(2)过氧化氢的浓溶液与氢氧化钡作用;
(3)氧化银在碱性介质中氧化过氧化氢;
(4)二价锰离子催化分解过氧化氢;
(5)高锰酸钾的酸性溶液与过氧化氢作用;
(6)在高温下硫单质与碳作用;
(7)点燃硫粉与铁粉的混合物;
(8)单质硫置于氢氧化钠中共热;
(9)硫化氢与单质溴反应;
(10)将硫化氢气体通入三价铁离子的溶液中;
(11)单质铜与浓硫酸作用;
(12)二硫化锡、硫化汞分别溶于硫化钠溶液中;
(13)以五氧化二钒为催化剂利用空气中的氧气氧化二氧化硫;
(14)隔绝空气加热亚硫酸钠固体;
(15)硫酸氢钠受强热脱水;
(16)灼烧过的氧化铝与焦硫酸钾共熔;
(17)氯磺酸与水作用;
(18)沸腾的亚硫酸钠溶液与硫粉反应;
(19)向硫化钠和碳酸钠的混合溶液中通入二氧化硫气体;
(20)溴化银溶于硫代硫酸钠溶液中;
(21)过二硫酸钾受热分解;
(22)碲化铝的水解;
(23)过氧化氢氧化二氧化碲。