 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
合成氨反应N2+3H2=2NH3,若N2起始浓度为1mol/L,经过2s后变为0.8mol/L,以反应进度表示反应速率,则NH3的反应速率为:()。
A.0.1mol・L-1・s-1
B.0.2mol・L-1・s-1
C.0.3mol・L-1・s-1
D.1mol・L-1・s-1
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.0.1mol・L-1・s-1
B.0.2mol・L-1・s-1
C.0.3mol・L-1・s-1
D.1mol・L-1・s-1
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“合成氨反应N2+3H2=2NH3,若N2起始浓度为1mol/…”相关的问题
更多“合成氨反应N2+3H2=2NH3,若N2起始浓度为1mol/…”相关的问题
反应N2(g)+3H2(g)=2NH3(g)(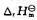 >0)达到平衡后采取下列哪种方法能使平衡向有移动。()
>0)达到平衡后采取下列哪种方法能使平衡向有移动。()
A.加入催化剂
B.降低温度
C.增加H2的压力
D.降低系统的总压
已知下列反应△rHΘm值的正、负,判断反应在高温和低温时的自发状态。 (1)2Fe(S)+3/2O2(g)=Fe2O3(s) △rHΘm<0 (2)2NH3(g)=N2(g)+3H2(g) △rHΘm>0 (3)C2H5OH(1)=C2H5OH(g) △rHΘm>0 (4)2Cl2(g)+7O2(g)=2Cl2O7(l) △rHΘm>0 (5)C2H5OH(l)+2O2(g)=2CO2(g)+3H2O(g) △rHΘm<0
在氧化还原滴定中,若氧化剂和还原剂两个半电池反应中,转移的电子数相等,即n1=n2,则计量点应在滴定突跃的______;若n1≠n2,则计量点偏向电子转移数______的电对一方。
根据298.15K,pΘ时物质的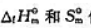 值,(1)求下列反应CO2(g)+2NH3(g)=CO(NH2)2(s)+H2O(l)的
值,(1)求下列反应CO2(g)+2NH3(g)=CO(NH2)2(s)+H2O(l)的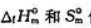 ;(2)计算上述反应在298.15K及pΘ下的ΔrGΘm值,.并判断由CO2(g)和NH3(g)反应生成尿素是否为自发过程.
;(2)计算上述反应在298.15K及pΘ下的ΔrGΘm值,.并判断由CO2(g)和NH3(g)反应生成尿素是否为自发过程.
合成氨反应:

在30.4MPa,500℃时,K为7.8×10-5,计算该温度时下列反应的K: