 更多“电解时,任一物质在电极上析出的量及通过电解池的()成正比。”相关的问题
更多“电解时,任一物质在电极上析出的量及通过电解池的()成正比。”相关的问题
第1题
在锌电极上析出氢气的Tafel公式为 η/V=0.72+0.116lg[j/(A·cm-2)] 在298K时,用Zn(s)作阴极,惰性物质作阳极
在锌电极上析出氢气的Tafel公式为
η/V=0.72+0.116lg[j/(A·cm-2)]
在298K时,用Zn(s)作阴极,惰性物质作阳极,电解浓度为0.1mol·kg-1的ZnSO4溶液,设溶液pH值为7.0,若要使H2(g)不和锌同时析出,应控制什么条件?
第2题
下列关于铜电极的叙述正确的是()
A.用电解法精炼粗铜时粗铜与外部电源负极相连
B.用电解法精炼粗铜时粗铜作阴极
C.在镀件上电镀铜时用金属铜作阳极
D.电解稀硫酸制H2、O2时铜作阳极
E.用惰性电极电解稀CuCl2溶液,最初一段时间阴极和阳极上析出的物质分别是
第4题
用两个银电极电解AgNO3,水榕液时,当电路中通过的电荷量为1F时,在阴极会析出()mol的银.
用两个银电极电解AgNO3,水榕液时,当电路中通过的电荷量为1F时,在阴极会析出()mol的银.
点击查看答案
第6题
25℃时,某溶液中含有Ag(a1=0.05),Cd2+(a2=0.001),Ni2+(a3=0.1)和H+(a4=0.001),且已知H2(g)在Pt、Ag、Cd及Ni上
25℃时,某溶液中含有Ag(a1=0.05),Cd2+(a2=0.001),Ni2+(a3=0.1)和H+(a4=0.001),且已知H2(g)在Pt、Ag、Cd及Ni上的超电势分别为0.12V、2.0V、0.3V及0.24V。用Pt电极电解上述溶液,当外加电压从零开始逐渐增加时,在阴极上依次发生什么反应?假定在Pt等金属上析出上述各种金属的超电势可忽略不计。
第7题
在含有1.000 mol?L-1硫酸锌与1.000 mol?L-1硫酸镉的1.0 mol?L-1的硫酸介质中,进行电解实验。试计
在含有1.000 mol?L-1硫酸锌与1.000 mol?L-1硫酸镉的1.0 mol?L-1的硫酸介质中,进行电解实验。
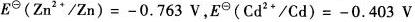 试计算:(1)电解时,锌和镉何者先析出? (2)能否在实验中完全分离锌和镉? (3)在铂和汞电极上,氢的析出是否干扰锌和镉的析出?(已知在铂和汞电极上的ηH2分别为一0.2 V和一1.0 V,ηZn和ηcd均为零)。
试计算:(1)电解时,锌和镉何者先析出? (2)能否在实验中完全分离锌和镉? (3)在铂和汞电极上,氢的析出是否干扰锌和镉的析出?(已知在铂和汞电极上的ηH2分别为一0.2 V和一1.0 V,ηZn和ηcd均为零)。
第8题
某试液含有1.000 m?L -1 Cu2+和1.000×10-2mol?L-1Ag+,若以铂电极进行电解,在阴极上首先析出的是
某试液含有1.000 m?L -1 Cu2+和1.000×10-2mol?L-1Ag+,若以铂电极进行电解,在阴极上首先析出的是铜还是银?两种离子是否可以电解分离?(
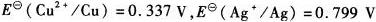 )
)
第9题
用铂电极电解CuCl2溶液.通过的电流为20A,经过15min后,问; (1)在阴极上能析出多少质量的Cu?(2)在27℃,100kPa下.阳极上能析出多少体积的Cl2(g)?
用铂电极电解CuCl2溶液.通过的电流为20A,经过15min后,问; (1)在阴极上能析出多少质量的Cu?(2)在27℃,100kPa下.阳极上能析出多少体积的Cl2(g)?
点击查看答案
第10题
用两支铂电极组成一电解池,电解池的内阻为0.50 Ω,铂电极的面积均为150 cm2。将两支铂电极分别插入
200.00 mL 0.500 mol?L-1 H2SO4和0.100 mol?L-1CuSO4溶液中进行电解,如果通入的电解电流为1.00 A,计算开始沉积Cu2+时需要的外加电压为多少?(已知
点击查看答案
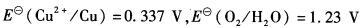 O2在Pt电极上的超电位为0.85 V,Cu的超电位为0 V)
O2在Pt电极上的超电位为0.85 V,Cu的超电位为0 V)
第11题
在电解分析时,金属离子析出的实际分解电压要比理论分解电压要______,其主要原因是当有电流流过时,电极极化
所致。极化使得阴极电位φ-更______,阳极电位φ+更______,相应产生______和______。另外,外加电压还应包括电解池的电压降iR。所以实际分解电压U实=______。
点击查看答案


 如果结果不匹配,请
如果结果不匹配,请 

















