 更多“通过重氮盐的放氮反应可以制备()”相关的问题
更多“通过重氮盐的放氮反应可以制备()”相关的问题
解释下列反应的原理: (a)二氢与液态植物油通过加氢反应制备人造黄油 (b)电解水的过程中可以富集重水 (c)化合物用氘标记后可以研究其反应机理 (d)Pd/Ag合金管用于纯化二氢 (e)CaH2可以作为干燥剂
A.易制备和提纯,较为稳定
B.一般具有较深的颜色(在可见区内的吸收系数大于1051mol-1.cm-1);
C.分子平面性使其固态结构有自我取向的趋势
D.分子固体的半导体性能显著
E.通过适当的掺杂可以改变其导电性
F.其基态和激发态与适当环境可发生氧化还原反应
A.化学吸收
B.在精馏塔里进行由甲醇和醋酸制备醋酸甲酯的过程
C.分离沸点相近的混合物的萃取结晶过程
D.催化精馏过程
利用标准摩尔生成吉布斯自由能数据,分析298.15K时,通过以下两组反应制备苯胺的可能性.
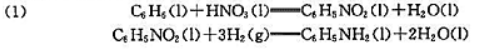
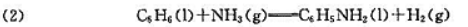
已知:
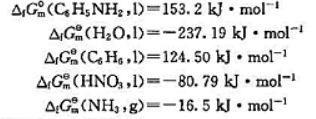
【题目描述】
19.(12分)
某实验小组利用如下装置(部分固定装置略)制备氮化钙(Ca3N2),并探究其实验式。

(1)按图连接好实验装置。检查装置的气密性,方法是。
(2)反应过程中末端导管必须插入试管A的水中,目的是。
(3)制备氮化钙的操作步骤是:①打开活塞K并通入N2;②点燃酒精灯,进行反应;③反应结束后,;④拆除装置,取出产物。
(4)数据记录如下:

① 计算得到实验式CaxN2,其中x=.
② 若通入的N2中混有少量O2,请比较x与3的大小,并给出判断依据:。
【我提交的答案】:fghfd
【参考答案分析】:【答案】(1)关闭活塞,微热反应管,试管A中有气泡冒出,停止加热。冷却后若末端导管中水柱上升且高度保持不变,说明装置气密性良好。
(2)防止反应过程中空气进入反应管,便于观察N2的逆流
(3)熄灭酒精灯,待反应管冷却至室温,停止通入氮气,并关闭活塞。
(4)①2.80 ②产物中生成了CaO
【解析】(1)见答案;(2)要保证整个装置不能混入其他气体;(3)一定要使玻璃管冷却后再停止通入气流;(4)要确定X值必须求出钙和氮的原子个数比根据题目给的数据可做如下计算①m(Ca)=(15.08-14.80)g=0.28g,m(N)= (15.15-15.08)g=0.07g,则n(Ca):n(N)=0.28/40 :0.07/14=7:5,则x=14/5;②若通入的N2中混有少量O2,则产物中就有可能混有了CaO,而Ca3N2中钙的质量分数为81.08﹪,CaO中钙的质量分数为71.43﹪,所以产物中混有了CaO会导致钙的质量分数减小,x的值偏小。
【我的疑问】(如下,请求专家帮助解答)
U形管的作用
A.“湿法炼铜”的化学原理可以表示为Fe+CuSO4===FeSO4+Cu
B.电解氯化镁可以制备金属镁,该反应为分解反应
C.工业上用一氧化碳还原氧化铁制备铁,该反应属于置换反应
D.金矿中的金是以单质形式存在,用物理方法可以制得


 如果结果不匹配,请
如果结果不匹配,请 

















