 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
HAc的pKa=4.76,苯甲酸C6H5COOH的Ka=4.19,HCOOH的pKa=3.75,HCN的pKa=9.21,据此,不能用标准碱溶液直接滴定0.1mol/L的酸应是:()。
A.HCl
B.HAc
C.C6H5COOH
D.HCOOH
E.HCN
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.HCl
B.HAc
C.C6H5COOH
D.HCOOH
E.HCN
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“HAc的pKa=4.76,苯甲酸C6H5COOH的Ka=4.…”相关的问题
更多“HAc的pKa=4.76,苯甲酸C6H5COOH的Ka=4.…”相关的问题
A.8.77~9.70
B.7.77~9.70
C.6.77~9.70
D.7.77~10.70
HAc 的 ρK.= 4.74 , 用它配制缓冲溶液的 pH 缓冲范围是() , NH3 的 ρKb= 4.76 ,其配制缓冲榕液的 pH 缓冲范围是()。
298K下,0.2mol·L-1的HAc溶液与0.2mol·L-1的NaAc溶液等体积混合后,该溶液的pH为() , 已知:HAc的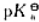 =4.76
=4.76
A.HCOOH—HCOONa(pKa=3.76)
B.H3PO4—NaH2PO4(pKa1=2.13)
C.HAc—NaAc(pKa= 4.75)
D.H2C8H4O4—KHC8H4O4(pKa1=2.95
A.4.75
B.6.25
C.7.00
D.9.25
A.NaHCO3-Na2CO3(H2CO3的pKa2=10.35)
B.HAc-NaAc(HAc的pKa=4.75)
C.Na2HPO4-Na3PO4(H3PO4的pKa3=12.36)
D.NH4Cl-NH3·H2O(NH3·H2O的pKb=4.75)
A.NaHCO3-Na2CO3(H2CO3的pKa2=10.35)
B.HAc-NaAc(HAc的pKa=4.75)
C.Na2HPO4-Na3PO4(H3PO4的pKa3=12.36)
D.NH4Cl-NH3·H2O(NH3·H2O的pKb=4.75)
在下列电池中Pt,H2(101.3kPa),HAc(xmol.L-1),Ac一(ymol.L-1)SCE当电池的电动势为0.620 V时,计算溶液中[HAe]和[NaAc]的比值为多少(25℃)?(已知E(SCE)=0.242 V,醋酸的pKa=4.74)
钾长石试样0.5000g,经分析处理得0.1834g K[B(C6H5)4]。计算钾长石中K2O的含量。