 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在一定温度下。当 反应达到平衡状态时,生成物浓度相应幂次的乘积与反应物浓度相应幂次的乘积 是一个常数。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“ 在一定温度下。当 反应达到平衡状态时,生成物浓度相应幂次的…”相关的问题
更多“ 在一定温度下。当 反应达到平衡状态时,生成物浓度相应幂次的…”相关的问题
任何可逆反应在一定温度下,不论参加反应的物质的起始浓度如何,反应达到平衡时,各物质的平衡浓度相同。( )
已知反应 的标准摩尔焓变
的标准摩尔焓变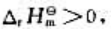 ,在一定温度下达到平衡状态。欲使N2O4的解离度增大,可采取的措施是()。
,在一定温度下达到平衡状态。欲使N2O4的解离度增大,可采取的措施是()。
A、将系统的体积压缩为原来的1/2
B、体积保持不变,加入惰性气体使压力增大到原来的2倍
C、压力保持不变,加入惰性气体使体积增大到原来的2倍
D、体积保持不变,加入NO气体使压力增大到原来的2倍
A. 化学平衡状态是正逆反应都停止的状态
B. 对于可逆反应C(s)+ H20(g) = CO(g) + H2(g),在一定温度下达到平衡,ρ(H20)=ρ(CO)=ρ(H2) ,即反应物与生成物压力相等
C. 反应N2(g) +02(g) =2NO(g)和2N2(g) +202(g) =4NO(g)虽代表同一反应,但是它们的标准平衡常数不相等
D. 多步反应的总标准平衡常数为各步反应标准平衡常数之和
将物质的量相等的CO和H2O(g)混合于一容器中,发生下列反应: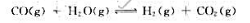 在一定温度下达到化学平衡时.CO的平衡转化率为α,则上述反应的标准平衡常数
在一定温度下达到化学平衡时.CO的平衡转化率为α,则上述反应的标准平衡常数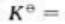 ()平衡时系统的总压力与反应开始时的总压力相比,将();压缩系统的体积时,化学平衡将();若在系统的总压力不变的条件下加入惰性气体,化学平衡将()。
()平衡时系统的总压力与反应开始时的总压力相比,将();压缩系统的体积时,化学平衡将();若在系统的总压力不变的条件下加入惰性气体,化学平衡将()。
对反应 ,在一定温度和浓度下,无论使用催化剂或不使用催化剂,只要反应达到平衡,产物的浓度总是相同的。( )
,在一定温度和浓度下,无论使用催化剂或不使用催化剂,只要反应达到平衡,产物的浓度总是相同的。( )
在500K时将 在体积为15.0L的容器内达到下列化学平衡:
在体积为15.0L的容器内达到下列化学平衡: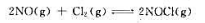 当反应在500K达到化学平衡后测得容器内NaCl的物质的量为3.06mol,计算该温度下NO的平衡物质的量和反应的标准平衡常数。
当反应在500K达到化学平衡后测得容器内NaCl的物质的量为3.06mol,计算该温度下NO的平衡物质的量和反应的标准平衡常数。
可逆反应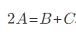 在一定条件下达到平衡时,若升高温度,平衡向左移动,则正反应为______反应。B为气体,增大压强,平衡若向右移动,则C为______体。
在一定条件下达到平衡时,若升高温度,平衡向左移动,则正反应为______反应。B为气体,增大压强,平衡若向右移动,则C为______体。
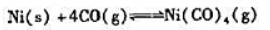
(1)不查附表,判断该反应是嫡增反应还是煽减反应.
(2)在某温度下该反应自发进行,推测反应自发进行时环境的璃是增加还是减少.
(3)利用附表一中所查到的数据,计算25℃下该反应的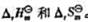
(4)当该反应的时,温度为多少?
(5)在提纯镍的Mond过程中,第一步是粗镍与CO,Ni(CO)4(四羰基合镍)在50℃左右的温度下达到平衡,这一步的标准平衡常数应尽可能的大,以便使镍充分地变成气相化合物.计算50℃下上述反应的标准平衡常数Kθ.
(6)在Mond过程中的第二步,将气体混合物从反应器中除去,并将其加热至230℃左右.在足够高的温度下的正、负号可以转换,反应在相反方向上发生,沉积出纯镍.在这一步,前述反应的标准平衡常数应尽可能的小.计算在230℃下该反应的标准平衡常数.
(7)Mond过程的成功依赖于Ni(CO)4的挥发性.在室温条件下,Ni(CO)4是液体,42.2℃时沸腾,其汽化焓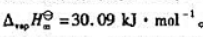 计算该化合物的汽化熵
计算该化合物的汽化熵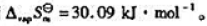
(8)近来改进了的Mond过程是在较高压力和150℃下进行第一步反应的.估算150℃下,Ni(CO)4,将要液化之前所能达到的最大压力(即估算150℃下,Ni(CO)4(l)的蒸气压).
反应Sn+Pb2+═Sn2++Pb在298K达到平衡,该温度下Kc=2.18。若反应开始时c(Pb2+)=0.1mol/L,c(Sn2+)=0.1mol/L,计算平衡时Pb2+之和Sn2+浓度。
在950℃时,可逆反应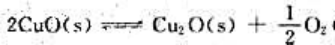 的标准平衡常数
的标准平衡常数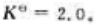 则在此温度下上述反应达到平衡时O2的分压为()。
则在此温度下上述反应达到平衡时O2的分压为()。
A、1.4kPa
B、4.0kPa
C、140kPa
D、400kPa