 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知水蒸气的压力P和温度T,在该温度当P小于P饱和时,介质处于()状态。
A.饱和空气
B.温蒸汽
C.干蒸汽
D.过热蒸汽
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.饱和空气
B.温蒸汽
C.干蒸汽
D.过热蒸汽
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知水蒸气的压力P和温度T,在该温度当P小于P饱和时,介质处…”相关的问题
更多“已知水蒸气的压力P和温度T,在该温度当P小于P饱和时,介质处…”相关的问题
已知水(H2O,I)在100℃的饱和蒸气压p=101.325kPa,在此温度.压力下水的摩尔蒸发焓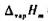 =40.668kJ·mol-1.求在100℃,101.325kPa下使1kg水蒸气全部凝结成液体水时的Q,W,ΔU和ΔH.设水蒸气适用理想气体状态方程.
=40.668kJ·mol-1.求在100℃,101.325kPa下使1kg水蒸气全部凝结成液体水时的Q,W,ΔU和ΔH.设水蒸气适用理想气体状态方程.
已知环己烷(1)-苯(2)系统在40℃时的活度系数模型为GE=0.458RTx1x2,纯组分的蒸气压为p
通用压缩因子图描述了实际气体压缩因子z=f(pr,tr)的函数关系式,试简述利用通用压缩因子图,在已知实际气体的温度T和比体积v的情况下求取压力p的步骤。
A.0.152
B.0.167
C.0.174
D.0.185
某二元混合物,在T,p时,其摩尔体积表达式为
V=90x1+50x2+(6x1+9x2)x1x2
其中V的单位是cm3/mol。试确定在该温度压力下:
(1)用x1表示
(2)无限稀释下
(3)作V-x1图,在图上标出V1,V2,
在常温真实溶液中,溶质B的化学势可表示为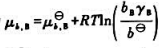 ,式中B的标准态为温度T、压力p=pθ=100kPa下,
,式中B的标准态为温度T、压力p=pθ=100kPa下,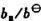 =(),
=(),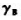 =(),同时又遵循亨利定律的假想态.
=(),同时又遵循亨利定律的假想态.
已知乙醇(1)-丙酮(2)-氯仿(3)三元均相恒沸物,求其恒沸温度为63.2℃时的压力和恒沸组成。Wilson参数(J/mol)如下:g12-g11=1085.2056;g21-g22=958.4808;g23-g22=-34.8727;g32-g33=-1836.2191;g13-g11=5866.3043;g31-g33=-1213.7747。 液体摩尔体积νiL=ai+biT+ciT2(νiL,cm3/mol;T,K)
 安托尼公式(P0,Pa;T,K):乙醇InP10=23.8047-3803.98/(T-41.68) 丙酮lnp20=21.5441-2940.46/(T-35.93) 氯仿lnp30=20.8660-2696.79/(T-46.16) (文献值:p=101.3kPa,x1=0.189,x2=0.350)
安托尼公式(P0,Pa;T,K):乙醇InP10=23.8047-3803.98/(T-41.68) 丙酮lnp20=21.5441-2940.46/(T-35.93) 氯仿lnp30=20.8660-2696.79/(T-46.16) (文献值:p=101.3kPa,x1=0.189,x2=0.350)
在T、P为常数时,曾有人推荐用下面一对方程来表示二元系偏摩尔体积数据:
式中,a、b是温度和压力的函数,试问从热力学角度考虑,上述方程是否合理?
呼吸期间CO2从静脉进入肺泡,后被排出。在肺泡中CO2的压力P(t)服从
温度和压力对吸收的影响为:
a、T增大P减小,Y2增大X1减小
b、T减小P增大,Y2减小X1增大
c、T减小P增大,Y2增大X1减小
d、T增大P减小,Y2增大X1增大