 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列电池的电动势为0.048V,计算AgI的溶度积常数=? (Ag[+/Ag)=+0.799V] (-)Ag,AgI(s)|NaI(0.020mol·L-1)||
下列电池的电动势为0.048V,计算AgI的溶度积常数![下列电池的电动势为0.048V,计算AgI的溶度积常数=? (Ag[+/Ag)=+0.799V]](https://img2.soutiyun.com/ask/uploadfile/5127001-5130000/b322179d9ec174367071fcdcc7732dd9.png) =?
=?
![下列电池的电动势为0.048V,计算AgI的溶度积常数=? (Ag[+/Ag)=+0.799V]](https://img2.soutiyun.com/ask/uploadfile/5127001-5130000/c8b99d637dc3d8a47d3d005b0c8eaab4.png) (Ag[+/Ag)=+0.799V]
(Ag[+/Ag)=+0.799V]
(-)Ag,AgI(s)|NaI(0.020mol·L-1)||H+(a=1mol·L-1)|H2(101.325kPa)|Pt()。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列电池的电动势为0.048V,计算AgI的溶度积常数![下列电池的电动势为0.048V,计算AgI的溶度积常数=? (Ag[+/Ag)=+0.799V]](https://img2.soutiyun.com/ask/uploadfile/5127001-5130000/b322179d9ec174367071fcdcc7732dd9.png) =?
=?
![下列电池的电动势为0.048V,计算AgI的溶度积常数=? (Ag[+/Ag)=+0.799V]](https://img2.soutiyun.com/ask/uploadfile/5127001-5130000/c8b99d637dc3d8a47d3d005b0c8eaab4.png) (Ag[+/Ag)=+0.799V]
(Ag[+/Ag)=+0.799V]
(-)Ag,AgI(s)|NaI(0.020mol·L-1)||H+(a=1mol·L-1)|H2(101.325kPa)|Pt()。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列电池的电动势为0.048V,计算AgI的溶度积常数=? …”相关的问题
更多“下列电池的电动势为0.048V,计算AgI的溶度积常数=? …”相关的问题
测得电池Zn|ZnCl2(a=0.05)|AgCl(s)|Ag的电动势在298.15K时为1.015V,温度系数TCR为-4.92×10-4V/K,试写出电池反应并计算当电池可逆放电2mol电子电量时,电池反应的△rGm、△rSm、△rHm及电池的可逆热Qr。
电池Ag(s)AgCl(s)]KCl(m)|Hg2Cl2(s)|HIg(I)的电池反应为
Ag(s)+1/2Hg2CI2(s)→AgCl(s)+Hg(I),已知298K时,此电池反应的焓变![电池Ag(s)AgCl(s)]KCl(m)|Hg2Cl2(s)|HIg(I)的电池反应为Ag(s)+](https://img2.soutiyun.com/ask/2020-11-21/974838996162397.png) 为5435/mol,各物质的规定熵数据为
为5435/mol,各物质的规定熵数据为
![电池Ag(s)AgCl(s)]KCl(m)|Hg2Cl2(s)|HIg(I)的电池反应为Ag(s)+](https://img2.soutiyun.com/ask/2020-11-21/974839108195805.png) 试计算该温度下电池的电动势E及电池电动势的温度系数
试计算该温度下电池的电动势E及电池电动势的温度系数![电池Ag(s)AgCl(s)]KCl(m)|Hg2Cl2(s)|HIg(I)的电池反应为Ag(s)+](https://img2.soutiyun.com/ask/2020-11-21/974839124694749.png)
测得电池Zn(S)|ZnCl2(a=0.05)|AgCl(s)|Ag(s)的电动势在298K时为1.015V,温度系数
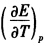 为-4.92×10-4V/K,试写出电池反应并计算当电池有2mol电子电量输出时,电池反应的△rGm、△rSm、△rHm及电池的可逆热Qr。
为-4.92×10-4V/K,试写出电池反应并计算当电池有2mol电子电量输出时,电池反应的△rGm、△rSm、△rHm及电池的可逆热Qr。
25℃时测得下列电池的电动势为0.622V,求配合物Ag(CN)2-的稳定常数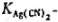 。(已知
。(已知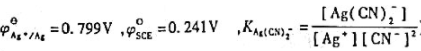 )
)
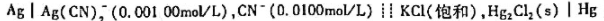
计算Pt(s)|Fe2+(c=0.10 mol.dm-3),Fe3+(c=0.20 mol.dm-3)‖Ag+(c=1.0 mol.dm-3)|Ag(s)的电池电动势。
在298K时,有电池:Ag(s)|AgCl(s)|NaCl(aq)|Hg2Cl2(s)|Hg(l)。已知化合物的标准生成Gibbs自由能分别为

普通水泥在固化过程中其自由水分子减少并形成碱性溶液。根据这一物理化学特点,科学家发明了电动势法测水泥的初凝时间。此法的原理如图所示,反应的总方程式为:2Cu+Ag2O=Cu2O+2Ag。下列有关说法正确的是()。
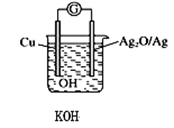
A.2molCu与1molAg2O的总能量低于1molCu2O与2molAg具有的总能量
B.
负极的电极反应式为2Cu+2OH--2e-=Cu2O+H2O
C.测量原理示意图中,电流方向从Cu流向Ag2O
D.电池工作时,OH-向Ag电极移动