 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
讨论下列性质: (1)Ln(OH)3的碱强度随Ln原子序数的提高而降低。 (2)镧系元素为什么形成配合
讨论下列性质: (1)Ln(OH)3的碱强度随Ln原子序数的提高而降低。 (2)镧系元素为什么形成配合物的能力很弱?镧元素配合物中配位键为什么主要是离子性的? (3)Ln3+大部分是有色的、顺磁性的。
 答案
答案
(1)Ln(OH)3为离子型碱性氢氧化物随着离子半径的减小中心离子对OH-的吸引力增强其碱性减弱即由La(OH)3到Lu(OH)3碱性递减。总的来说碱性比Ca(OH)2弱但比Al(OH)3强容易与无机酸反应生成相应的盐。
(2)Ln3+电荷虽高但半径较大因而离子势较小。基态Ln3+具有稀有气体原子的外层电子结构(5s25p6)内层4f轨道与外部原子的扰动隔绝受外部原子的影响较小因而内层4f电子受周围配位体电场的影响较小它们之间相互作用很弱4f轨道参与成键的成分不大。化学键具有一定共价性的主要贡献来自外层的5d和6s轨道。Ln3+与配位体之间相互作用是以静电作用为主。因此镧系元素形成配位化合物的倾向很小Ln3+与配位体之间的相互作用以静电作用为主所形成的配位键主要是离子性的。
(3)f区元素的离子显色大多是由f-f、f—d跃迁及荷移跃迁引起的。
+3价镧系元素离子的4f电子可以在7个4f轨道之间任意分布从而产生多种多样的电子能级因而Ln3+大部分是有色的吸收光谱极为复杂。Ln3+的颜色变化大致有以下特点:①具有fx和f14-x(x=12…7)构型的离子显示的颜色常相同或相近;②具有f0、f7、f14(全空、半满、全满)结构的离子是无色的;③成单电子数为2~5的离子都是有色的且成单电子数相同的离子所显示的颜色也是相似的。
根据顺磁性物质含有未成对电子、反磁性物质不含未成对电子的原则4f0构型的La3+和Ce4+以及4f14构型的Yb2+和Lu3+没有未成对电子因此都是反磁性的而f1-13构型的离子或原子都是顺磁性的。Ln3+核外未成对电子数多因此Ln3+大部分是顺磁性的。并且大多数+3价离子磁矩比d过渡元素离子的大。Ln3+的磁矩与电子的自旋运动和轨道运动均有关对于镧系离子Ln3+来说由于外层5s25p6电子的屏蔽作用4f电子受配体场的影响较小。
(1)Ln(OH)3为离子型碱性氢氧化物,随着离子半径的减小,中心离子对OH-的吸引力增强,其碱性减弱,即由La(OH)3到Lu(OH)3碱性递减。总的来说,碱性比Ca(OH)2弱,但比Al(OH)3强,容易与无机酸反应生成相应的盐。(2)Ln3+电荷虽高,但半径较大,因而离子势较小。基态Ln3+具有稀有气体原子的外层电子结构(5s25p6),内层4f轨道与外部原子的扰动隔绝,受外部原子的影响较小,因而内层4f电子受周围配位体电场的影响较小,它们之间相互作用很弱,4f轨道参与成键的成分不大。化学键具有一定共价性的主要贡献来自外层的5d和6s轨道。Ln3+与配位体之间相互作用是以静电作用为主。因此,镧系元素形成配位化合物的倾向很小,Ln3+与配位体之间的相互作用以静电作用为主,所形成的配位键主要是离子性的。(3)f区元素的离子显色大多是由f-f、f—d跃迁及荷移跃迁引起的。+3价镧系元素离子的4f电子可以在7个4f轨道之间任意分布,从而产生多种多样的电子能级,因而Ln3+大部分是有色的,吸收光谱极为复杂。Ln3+的颜色变化大致有以下特点:①具有fx和f14-x(x=1,2,…,7)构型的离子显示的颜色常相同或相近;②具有f0、f7、f14(全空、半满、全满)结构的离子是无色的;③成单电子数为2~5的离子都是有色的,且成单电子数相同的离子所显示的颜色也是相似的。根据顺磁性物质含有未成对电子、反磁性物质不含未成对电子的原则,4f0构型的La3+和Ce4+以及4f14构型的Yb2+和Lu3+没有未成对电子,因此都是反磁性的,而f1-13构型的离子或原子都是顺磁性的。Ln3+核外未成对电子数多,因此Ln3+大部分是顺磁性的。并且大多数+3价离子磁矩比d过渡元素离子的大。Ln3+的磁矩与电子的自旋运动和轨道运动均有关,对于镧系离子Ln3+来说,由于外层5s25p6电子的屏蔽作用,4f电子受配体场的影响较小。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案

 更多“讨论下列性质: (1)Ln(OH)3的碱强度随Ln原子序数的…”相关的问题
更多“讨论下列性质: (1)Ln(OH)3的碱强度随Ln原子序数的…”相关的问题
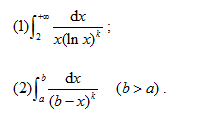
 ;(2)y=ln(1-x2);
;(2)y=ln(1-x2);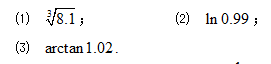
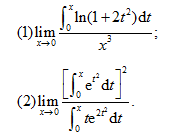
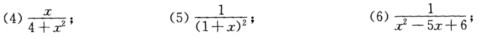 (7)(1+x)e-x;(8)arcsinx.
(7)(1+x)e-x;(8)arcsinx.
















