 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在PH为4.5的水溶液中,EDTA存在的主要形式是:()A.H4YB.H3Y-C.H2Y2-D.HY3-E.Y4-
在PH为4.5的水溶液中,EDTA存在的主要形式是:()
A.H4Y
B.H3Y-
C.H2Y2-
D.HY3-
E.Y4-
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在PH为4.5的水溶液中,EDTA存在的主要形式是:()
A.H4Y
B.H3Y-
C.H2Y2-
D.HY3-
E.Y4-
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在PH为4.5的水溶液中,EDTA存在的主要形式是:()A.…”相关的问题
更多“在PH为4.5的水溶液中,EDTA存在的主要形式是:()A.…”相关的问题
EDTA的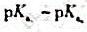 分别是0.9,1.6,2.0,2.67,6.16和10.26,EDTA二钠盐水溶液pH约是()。
分别是0.9,1.6,2.0,2.67,6.16和10.26,EDTA二钠盐水溶液pH约是()。
A.1.25
B.1.8
C.2.34
D.4.42
EDTA的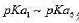 分别为0.9,1.6, 2.0,2.67,6.16, 10. 28,EDTA二钠盐水溶液的田pH约为()。
分别为0.9,1.6, 2.0,2.67,6.16, 10. 28,EDTA二钠盐水溶液的田pH约为()。
A.1.25
B.1.8
C.2.34
D.4.42
在pH=2的酸性溶液中,已知其中c(Fe3+)=0.010mol·L-1,c(Al3+)=0.010mol·L-1
(1)Al3+的存在是否干扰EDTA滴定Fe3+?(2)滴定Fe3+后的试液中,如果继续滴定Al3+,则试液允许的最低pH应多大?如何测定Al3+?
溶液中Mg2+的浓度为2.0×10-2mol/L,问:(1)pH=5.0时,能否用EDTA准确滴定Mg2+?(2)在pH =10.0时,情况如何?(3)继续升高pH情况又如何?
测定某试液中Fe2+、Fe3+的含量。吸取25.00mL该试液,在pH=10时用浓度为0.01500mol/L的EDTA标准溶液滴定,耗用15.40mL,调至pH=6,继续滴定,又耗用溶液体积14.10mL,计算两者的浓度(以mg/mL表示)。
欲测定ZnCl2的含量,先准确称取样品0.2500g,溶于水中后,在pH=6.0时以二甲酚橙为指示剂,用0.1024mol/L的EDTA标准溶液滴定,用去17.90mL,求试样中ZnCl2的质量分数。