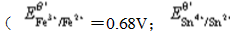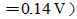题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
Al3+在0.1 mol?L-1HCl溶液中还原时,其极谱波的半波电位为一1.46 V。在滴汞电极电位为一1.70 V时,
Al3+在0.1 mol?L-1HCl溶液中还原时,其极谱波的半波电位为一1.46 V。在滴汞电极电位为一1.70 V时,测得溶液的电流值如下:
 根据以上极谱分析数据,计算Al3+的质量浓度(以mg?L-1为单位,已知M(A1)=26.98 g?mol-1。)。
根据以上极谱分析数据,计算Al3+的质量浓度(以mg?L-1为单位,已知M(A1)=26.98 g?mol-1。)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
Al3+在0.1 mol?L-1HCl溶液中还原时,其极谱波的半波电位为一1.46 V。在滴汞电极电位为一1.70 V时,测得溶液的电流值如下:
 根据以上极谱分析数据,计算Al3+的质量浓度(以mg?L-1为单位,已知M(A1)=26.98 g?mol-1。)。
根据以上极谱分析数据,计算Al3+的质量浓度(以mg?L-1为单位,已知M(A1)=26.98 g?mol-1。)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“Al3+在0.1 mol?L-1HCl溶液中还原时,其极谱波…”相关的问题
更多“Al3+在0.1 mol?L-1HCl溶液中还原时,其极谱波…”相关的问题
A.能使酚酞变红的溶液:Na+、Al3+、SO42-、NO3-
B.0.1 mol/LNaClO溶液:K+、Fe2+、Cl-、SO42-
C.0.1mol/L氨水:K+、Ag(NH3)2+、NO3-、OH-
D.由水电离产生的c(H+)=1×10-13 mol/L的溶液:Na+、NH4+、Cl-、HCO3-
【题目描述】
7.在下列各溶液中,离子一定能大量共存的是A.强碱性溶液中:K+、、Al3+、Cl-、SO2-4
B.含有0.1 mol·L-1Fe3+的溶液中:K+、Mg2+、I-、NO-3
C.含有0.1 mol·L-1Ca2+的溶液中:Na+、K+、CO2-3、Cl-
D.室温下,Ph=1的溶液中:Na+、Fe3+、NO-3、SO2-4
| 【我提交的答案】:C |
| 【参考答案与解析】: 正确答案:D |
答案分析:
【我的疑问】(如下,请求专家帮助解答)
D选项怎么解说,我对离子共存还不太了解
在100 mL 0.10 mol·L-1HCl中,用控制电位库仑法于一0.65 V(vs.SCE)测定0.045 8 mmol·L-1苦味酸。与电解池串联的库仑计测得其电量为75.4 C。计算此还原反应中的电子转移数n,并写出电极反应。
以2.0X10-2mol·L-1EDTA滴定浓度均为2.0X10-2mol·L-1的Al3+和Zn2+混合溶液中的Zn2+,在pH=5.5时,欲以KF掩蔽其中的Al3+,终点时游离KF的依度为1.0X10-8mol·L-1.计算说明在此条件下能否准确滴定Zn2+?已知:HF的pKθ=3.18;lgK(AIY)=16.1;lgKθ(ZnY)=16.5;pH=5.5时,
1ga[Y(H)]=5.5;AI3+-F-配合物的lgβ1θ~lgβ6θ分别为6.1,11.2,15.0,17.7,19.6,19.7.
A.饱和氯水中:Cl-、NO3-,Na+,SO3 2-
B.(H+)=1*10^-13 mol/L的溶液中:C6H5O-、K+,SO4 2-、Br-
C.硫化钠溶液中:SO4 2-,K+、Cl-、Cu2+
D.pH=12的溶液中:NO3 -、I-、Na+、Al3+
A.0.15 mol•L-1
B.0.2 mol•L-1
C.0.3 mol•L-1
D.0.4 mol•L-1
计算在1mol·L-1HCl溶液中,用Fe3+滴定Sn2+时化学计量点的电势,并计算滴定至99.9%和100.1%时的电势。说明为什么化学计量点前后,同样改变0.1%,电势的变化不相同。若用电势滴定判断终点,与计算所得化学计量点电势一致吗?