 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
某一级反应,300K时反应的半衰期为69.3min,400K时反应的半衰期为0.693min.试计算该反应的活化能。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某一级反应,300K时反应的半衰期为69.3min,400K…”相关的问题
更多“某一级反应,300K时反应的半衰期为69.3min,400K…”相关的问题
某化合物A的分解速率常数为0.29h-1,则此反应为______级反应,当c0=1.0mol·L-1时,此反应的半衰期为______,当c0=0.10mol·L-1时,此反应的半衰期为______。
已知300K时: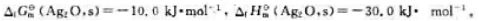
(1)试通过计算说明在300K、标准状态下、Ag2O(s)能否发生如下分解反应:
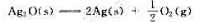
(2)计算在标准状态下Ag2O(s)发生分解反应的最低温度。
300K时,反应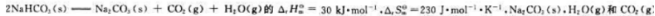 的标准摩尔生成吉布斯自由能AGR分别为-1044kJ·mol-1,-228kJ·mol-1和-393kJ·mol-1.试计算300K时NaHCO3(s)的标准摩尔生成吉布斯自由能.
的标准摩尔生成吉布斯自由能AGR分别为-1044kJ·mol-1,-228kJ·mol-1和-393kJ·mol-1.试计算300K时NaHCO3(s)的标准摩尔生成吉布斯自由能.
300K时,合成氨反应: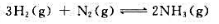 的温度范围内保持不变,计算该可逆反应在600K时的标准平衡常数。
的温度范围内保持不变,计算该可逆反应在600K时的标准平衡常数。
A.46.0kJ·mol-1
B.23.0kJ·mol-1
C.20.0kJ·mol-1
D.10.0kJ·mol-1
106J,请计算反应的Qp和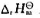 (WC,s,300K),已知C和w在300 K时的标准摩尔燃烧熔分别为-393.5kJ·mol-1和-837.5kJ·mol-1。
(WC,s,300K),已知C和w在300 K时的标准摩尔燃烧熔分别为-393.5kJ·mol-1和-837.5kJ·mol-1。
300K、标准状态下,C(石墨)—C(金刚石)的 在此条件下,该反应进行的方向是()
在此条件下,该反应进行的方向是()