 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
设在某一溶液中有两种物资,在反应开始时,两种物资的量分别为a和b;又设在时刻t,两种物资已经起反
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“设在某一溶液中有两种物资,在反应开始时,两种物资的量分别为a…”相关的问题
更多“设在某一溶液中有两种物资,在反应开始时,两种物资的量分别为a…”相关的问题
溶液中反应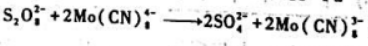 的速率方程为
的速率方程为
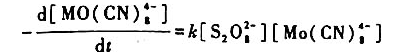
在20℃下,若反应开始时只有两反应物,且其初始浓度依次为0.01mol·dm-3,0.02mol.dm-3,反应26h后,测得[Mo(CN)34-]=0.01562mol.dm-3,求k.
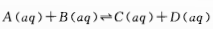 开始时只有A和B,经长时间反应,最终结果是()。
开始时只有A和B,经长时间反应,最终结果是()。A.C和D的浓度大于A和B的浓度
B. A和B的浓度大于C和D的浓度
C. A、B、C、D的浓度不再变化
D. A、B、C、D浓度相等
物资仓库网点的配置,只是确定仓库设在某一地区或某一城市,当这个问题确定之
后,就要进一步确定仓库在这一地区或城市的具体位置。这项工作就是地区选择。
当I2作为催化剂时,氯苯(C6H5Cl)与Cl2在CS2(1)溶液中发生如下的平行反应(均为二级反应):
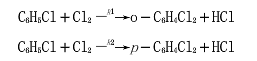
设在温度和I2的浓度一定时,C6H5Cl及Cl2在CS2(1)溶液中的起始浓度均为0.5mol·dm-3,30min后有15%的C6H5Cl转变为o-C6H4Cl2,有25%的C6H5Cl转变为p-C6H4Cl2,试计算两个速率常数k1和k2。
18. 溶液反应
20℃反应开始时只有两反应物,其初始浓度依次为0.01mol·dm-3和0.02mol·dm-3,反应26h后,测得
溶液反应的速率方程为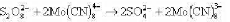 20°C,反应开始时只有两反应物,其初始浓度依次为0.01mol·dm-3,0.02mol·dm-3,反应20h后,测得
20°C,反应开始时只有两反应物,其初始浓度依次为0.01mol·dm-3,0.02mol·dm-3,反应20h后,测得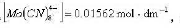 求k。
求k。
把CaCl2与Na2HPO4溶液混合时,可得磷酸八钙CasH2(PO4)6●5H2O晶体沉淀,把所得沉淀长时间加热可以水解生成羟基磷灰石结晶Cas(PO4)3(OH)。写出水解的反应方程式并讨论下列问题。
1.下列两种方法中,哪一种得到的羟基磷灰石多?为什么?
①1mol/dm3 CaCl2 50cm3 和1mol/dm3 Na2HPO4 30cm3 混合后,将所得
CagH2(PO4)6. 5H2O滤出。再将它放在80cm3水中于80°C加热5小时。
②lmol/dm3 CaCl2 50cm3和1mol/dm3 Na2HPO4 30cm3混合后,直接在80°C加热5小时。
2.在实验中,按①法制得的产物含Ca与含P摩尔比为1.5。计算CagH2(PO4)6中有多少摩尔百分比已转化为Cas(PO4)3(OH)?
某溶液中反应A+B→C,开始时反应物A与B的物质的量相等,没有产物C。1小时后A的转化率为75%,问2小时后A尚有多少未反应?假设:
(1)对A为一缴,对B为零级;
(2)对A、B皆为1级。