 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知K(HAc)=1.8×10-5,K(NH3·H2O)=1.8×10-5,为配制pH=4.5的缓冲溶液,可以选用下列溶液()。
A.HCl+NaOH
B.HAc+H2O
C.NH3·H2O+HCl
D.HCl+NaAc
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.HCl+NaOH
B.HAc+H2O
C.NH3·H2O+HCl
D.HCl+NaAc
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知K(HAc)=1.8×10-5,K(NH3·H2O)=1…”相关的问题
更多“已知K(HAc)=1.8×10-5,K(NH3·H2O)=1…”相关的问题
将1.00mol·dm-3HAc溶液和1.00mol·dm-3氢氟酸等体积混合,若已知HAc的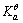 =1.8×10-5,HF的
=1.8×10-5,HF的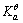 =6.3×10-4,试计算此溶液的c(H+),c(Ac-)和c(F-)。
=6.3×10-4,试计算此溶液的c(H+),c(Ac-)和c(F-)。
反应2SO2(g)+O2(g) 2SO3(g)在1000K时的KƟ=3.4×10-5,计算1100K时的KƟ。已知该反应的ΔrHƟm=-189kJ/mol,并设在此温度范围内ΔrHƟm只为常数。
2SO3(g)在1000K时的KƟ=3.4×10-5,计算1100K时的KƟ。已知该反应的ΔrHƟm=-189kJ/mol,并设在此温度范围内ΔrHƟm只为常数。
已知二元弱酸H2B的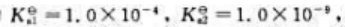 则二元弱碱B的K为().
则二元弱碱B的K为().
A、1.0×10-4
B、1.0×10-9
C、1.0×10-5
D、1.0×10-4
某NaAc·3H2O试样,欲以酸碱滴定法测定其含量,因HAc的Ka=1.8×10-5而不能直接滴定。若将其试液流经阳离子交换树脂柱,则______离子留于柱上,而______在流出液中,可用______直接滴定,并以______为指示剂。
已知25℃时,Ka(HAc)=1.75×10-5。计算该温度下0.10mol·L-1HAc溶液中H+浓度及溶液的pH,并计算该浓度下HAc的解离度。
求298K下,10mL 0.2mol·L-1的HAc溶液与10mL.0.2mol·L-1的NaAc溶液混合后。
(1)求该溶液的pH。
(2)若向此溶液中加入5mL0.01mol·L-1NaOH溶液,则溶液的pH又为多少?已知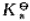 (HAc)=1.75×10-5。
(HAc)=1.75×10-5。
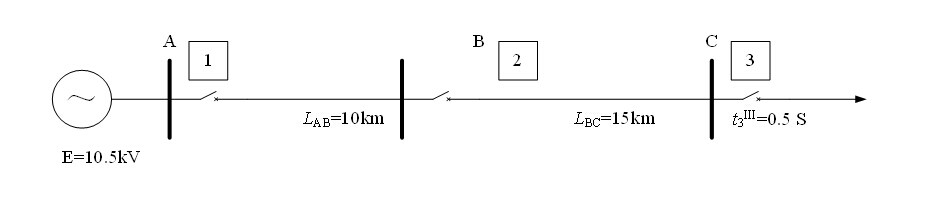
CMOS施密特与非门组成的电路如图7.3.3(a)所示,窄脉冲触发输入信号vI如图7.3.3(b)所示。已知R=5 kΩ,C=0.1μ F,VDD=5 V, VOH≈5 V,VILL≈0 V,VT+=3.3 V,VT-=1.8 V。 (1)分析电路的工作原理,画出vV及vO的波形(两个触发脉冲间隔的时间足够长)。 (2)计算输出高电平持续的时间。
1.jpg)