 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
有关2SO2(g)+O2(g)===(可逆)2SO3(g)的说法中,不正确的是()
A.该反应为可逆反应,故在一定条件下SO2和O2不可能全部转化为SO3
B.达到平衡后,反应就停止,故正、逆反应速率均为零
C.一定条件下,向某密闭容器中加入2 mol SO2和1 mol O2,则v正减小,v逆增大,直至v正=v逆
D.平衡时SO2、O2、SO3的分子数之比不再改变
 答案
答案
达到平衡后反应就停止故正逆反应速率均为零
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.该反应为可逆反应,故在一定条件下SO2和O2不可能全部转化为SO3
B.达到平衡后,反应就停止,故正、逆反应速率均为零
C.一定条件下,向某密闭容器中加入2 mol SO2和1 mol O2,则v正减小,v逆增大,直至v正=v逆
D.平衡时SO2、O2、SO3的分子数之比不再改变
 答案
答案
达到平衡后反应就停止故正逆反应速率均为零
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“有关2SO2(g)+O2(g)===(可逆)2SO3(g)的…”相关的问题
更多“有关2SO2(g)+O2(g)===(可逆)2SO3(g)的…”相关的问题
下列反应中,
(A) C(s)+O2(g)→CO2(g);
(B) 2SO2(g)+O2(g)→2SO3(g);
(C) 3H2(g)+N2(g)→2NH3(g);
(D) CuSO4(s)+5H2O(l)→CuSO4·5H2O(s)。
反应2SO2(g)+O2(g) 2SO3(g)在1000K时的KƟ=3.4×10-5,计算1100K时的KƟ。已知该反应的ΔrHƟm=-189kJ/mol,并设在此温度范围内ΔrHƟm只为常数。
2SO3(g)在1000K时的KƟ=3.4×10-5,计算1100K时的KƟ。已知该反应的ΔrHƟm=-189kJ/mol,并设在此温度范围内ΔrHƟm只为常数。
反应2SO2(g)+O2(g)=2SO3(g)在1000K时的KΘ=3.4×10-5,计算1100K时的KΘ。已知该反应的△rHmΘ=一189kJ/mol,并设在此温度范围内△rHmΘ为常数。
实验测得SO2氧化为SO3的反应,在1000K时,各物质的平衡分压为p(SO2)=27.7kPa、p(O2)=40.7kPa、p(SO3)=32.9kPa。计算该温度下反应2SO2(g)+O2(g)====2SO3(g)的平衡常数Kp。
A.容器中三氧化硫体积保持不变
B.容器中混合物的压强保持不变
C.混合物的总的物质的量保持不变
D.容器中SO2、O2与SO3的物质的量之比为2︰1︰2
应用教材附录中有关物质的热化学数据,计算25℃时反应
2CH3OH(I)+O2(g)=HCOOCH3(I)+2H2O(I)
的标准摩尔反应焓,要求:
(1)应用25℃的标准摩尔生成焓数据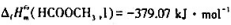 ;
;
(2)应用25℃的标准摩尔燃烧焓数据.
试从热力学原理说明直接氯化法从TiO2氯化制取TiCl4的可能性:
TiO2(s)+2Cl2(g)→TiCl4(1)+O2(g)
实际生产过程是在焦炭存在下高温氯化,请写出有关反应式并说明反应的基本原理,计算反应的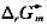 .
.
A.N2(g)+3H2(g)=2NH3(g)
B.2NO2(g)=N2O4(g)
C.2CO(g)+O2(g)=2CO2(g)
D.2NO(g)=N2(g)+O2(g)