 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在pH=5.0时用2x10-2mol/LEDTA滴定同浓度的Pb2+,以二甲酚橙为指示剂。计算终点误差。
①以HAc-NaAc缓冲溶液控制酸度,[HAc]=0.2mol/L,[Ac-]=0.4mol/L;②以六次亚甲基四胺缓冲溶液控制酸度。已知乙酸铅配合物的β1=101.9,β2=103.3;(CH2)6N4基本不与Pb2+配位。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在pH=5.0时用2x10-2mol/LEDTA滴定同浓度的…”相关的问题
更多“在pH=5.0时用2x10-2mol/LEDTA滴定同浓度的…”相关的问题
溶液中Mg2+的浓度为2.0×10-2mol/L,问:(1)pH=5.0时,能否用EDTA准确滴定Mg2+?(2)在pH =10.0时,情况如何?(3)继续升高pH情况又如何?
计算pH=5.0时Co2+和EDTA配合物的条件稳定常数(不考虑水解等副反应)。当Co2+抖浓度为0.02mol/L时,能否用EDTA准确滴定?
(1)计算pH=5.0时,H3PO4的分布系数δ3、δ2、δ1、δ0。(2)假定H3PO4各种形式的总浓度是0.050mol/L,问此时H3PO4,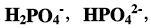
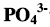 的浓度各为多少?
的浓度各为多少?
有一Zn2+、Mg2+混合溶液,通过计算说明在pH=5.0时可否滴定Zn2+而Mg2+不干扰?
当EDTA溶液的pH=5.0时,Y4-的lgαY(H)=6.45。若lgKCaY=10.69,则在pH=5.0时EDTA滴定Ca2+时的K'CaY=______。
欲测定ZnCl2的含量,先准确称取样品0.2500g,溶于水中后,在pH=6.0时以二甲酚橙为指示剂,用0.1024mol/L的EDTA标准溶液滴定,用去17.90mL,求试样中ZnCl2的质量分数。