 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
由标准钴电极(Co2+/Co)与标准氯电极组成原电池,测得其电动势为1.64V,此时钴电极为负极。已知(Cl2/Cl-)=1.36V
由标准钴电极(Co2+/Co)与标准氯电极组成原电池,测得其电动势为1.64V,此时钴电极为负极。已知 (Cl2/Cl-)=1.36V。问:(1) 标准钴电极的电极电势为多少(不查表)?(2) 此电池反应的方向如何?(3) 当氯气的压力增大或减小时,原电池的电动势将发生怎样的变化?(4) 当Co2+的浓度降低到0.010mol·dm-3时,原电池的电动势将发生怎样的变化?数值是多少?
(Cl2/Cl-)=1.36V。问:(1) 标准钴电极的电极电势为多少(不查表)?(2) 此电池反应的方向如何?(3) 当氯气的压力增大或减小时,原电池的电动势将发生怎样的变化?(4) 当Co2+的浓度降低到0.010mol·dm-3时,原电池的电动势将发生怎样的变化?数值是多少?
 答案
答案


 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案

 更多“由标准钴电极(Co2+/Co)与标准氯电极组成原电池,测得其…”相关的问题
更多“由标准钴电极(Co2+/Co)与标准氯电极组成原电池,测得其…”相关的问题
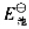 表示由上述两个电对组成的原电池的标准电动势,用K1和K2分别表示Co(OH)3和Co(OH)2的溶度积常数。试证明:
表示由上述两个电对组成的原电池的标准电动势,用K1和K2分别表示Co(OH)3和Co(OH)2的溶度积常数。试证明:
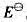 。
。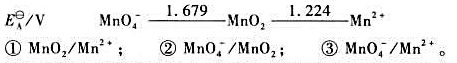
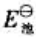 和电池反应的
和电池反应的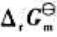 。
。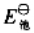 和电池反应的
和电池反应的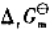 。
。
















