 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
当滴定反应为aA+bB→cC+dD时,被测物质B的质量。()
当滴定反应为aA+bB→cC+dD时,被测物质B的质量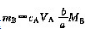 。( )
。( )
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
当滴定反应为aA+bB→cC+dD时,被测物质B的质量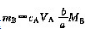 。( )
。( )
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“当滴定反应为aA+bB→cC+dD时,被测物质B的质量。()”相关的问题
更多“当滴定反应为aA+bB→cC+dD时,被测物质B的质量。()”相关的问题
A.化学计量数a与b一之和一定等于c与d之合
B.若取x克A和x克B反应生成C和D的质量总和一定是2x克
C.反应物A和B的质量比一定等于生成物C和D的质量比
D.若取x克A和x克B反应生成C和D的质量总和一定不是x2克
抗坏血酸(维生素C,摩尔质量为176.1g·mol-1)能被I2定量氧化,其反应为
C6H8O6+I2====C6H6O6+2HI
取100.0mL柠檬汁样品用H2SO4酸化,并加入20.00mL 0.02500mol·L-1I2溶液,待反应完全后,过量的I2用0.01000mol·L-1Na2S2O3标准溶液10.00mL滴定至终点,计算每毫升柠檬水果汁中抗坏血酸的质量。
抗坏血酸(摩尔质量为176.1g/mol)是一个还原剂,它的半反应为:
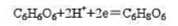
它能被I氧化,如果10.00ml柠檬水果汁样品用HAc酸化,并加20.00ml0.02500mol/LI2溶液,待反应完全后,过量的I2用1000ml0,01000mol/LNa2S2O3滴定,计算每毫升柠檬水果汁中抗坏血酸的质量。
用CLa(No3)3=0.03318mol?L-1的La(NO3)3溶液滴定100.0mL 0.03095mol?L-1的NaF的溶液,滴定反应为:
 ,用固体LaF。膜电极为指示电极(正极),饱和甘汞电极为参比电极(负级),测得其滴定数据为:
,用固体LaF。膜电极为指示电极(正极),饱和甘汞电极为参比电极(负级),测得其滴定数据为:
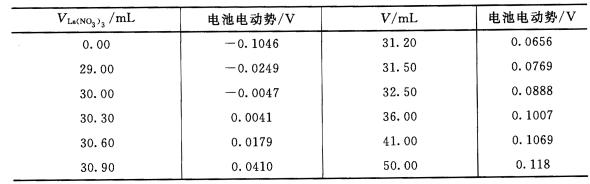 (1)计算反应完全时所需滴定剂的体积,并将其与电位滴定确定终点时消耗滴定剂的体积相比较。 (2)已知电池电动势与F一浓度的关系为:E=K+0.0592PF,用所测第一组数据算出K值。 (3)用求得的K值,计算加入50.00mI.,滴定剂后r的浓度?(设活度系数不变)
(1)计算反应完全时所需滴定剂的体积,并将其与电位滴定确定终点时消耗滴定剂的体积相比较。 (2)已知电池电动势与F一浓度的关系为:E=K+0.0592PF,用所测第一组数据算出K值。 (3)用求得的K值,计算加入50.00mI.,滴定剂后r的浓度?(设活度系数不变)
在0.1mol/L HCl溶液中,用Fe3+滴定Sn2+,其反应为
2Fe3++Sn2+====2Fe2++Sn4+