 更多“同一周期主族元素从左到右,电离能逐渐增大,即原子失电子能力逐…”相关的问题
更多“同一周期主族元素从左到右,电离能逐渐增大,即原子失电子能力逐…”相关的问题
同一周期的主族元素,从左到右,原子半径逐渐(),金属性逐渐()。
A.增大增强
B.增大减弱
C.减小减弱
D.减小增强
【题目描述】
第 2 题元素周期表是学习化学的重要工具。下面是元素周期表中1~18号元素原子核外电子排
布,我们对它进行研究:
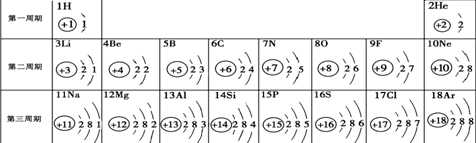
⑴ 第16号元素属于_______元素(填“金属”或“非金属”),它在化学反应中容易________(填“得”或“失”)电子;
⑵ 元素的化学性质与原子结构中的______________数关系密切;
⑶ 在同一族中,各元素的原子结构呈现的规律有________________ (任写一点);
⑷ 研究表明:第二周期从3~9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小。我分析第三周期从11~17号元素原子半径变化规律是 _________________________________。
【我提交的答案】:非金属 得 最外层电子数
【参考答案分析】:
⑴ 非金属 ;得 ;
⑵ 最外层电子 ;
⑶ 电子层数递增或最外层电子数相等或从上到下核电荷数增大等(只要合理均可)⑷ 逐渐减小
【我的疑问】(如下,请求专家帮助解答)
在同一族中,各元素的原子结构呈现的规律有________________ (任写一点);
⑷ 研究表明:第二周期从3~9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小。我分析第三周期从11~17号元素原子半径变化规律是 _________________________________。
A.旗形大多发生在市场极度活跃、股价运动近乎直线上升或下降的情况下
B.旗形分为上升旗形和下降旗形两种
C.旗形出现前,一般应有一个旗杆
D.旗形持续的时间不能太长,经验上,持续的时间应短于3周
E.旗形在形成过程中,成交量从左到右逐渐增大,被突破后,成交量更大
A.元素的核电荷数逐渐增大
B.元素的原子半径呈周期性的变化
C.元素的化合价呈现周期性变化
D.元素原子核外电子排布呈现周期性变化


 如果结果不匹配,请
如果结果不匹配,请 

















