 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
当下列电池中的标准溶液是pH=5.21的缓冲溶液时,在25℃时的电动势为0.209V。 玻璃电极|H+(a)||SCE。 当缓冲溶
当下列电池中的标准溶液是pH=5.21的缓冲溶液时,在25℃时的电动势为0.209V。
玻璃电极|H+(a)||SCE。
当缓冲溶液由待测试液代替时,测得的电动势为0.312V,计算待测试液的pH。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
当下列电池中的标准溶液是pH=5.21的缓冲溶液时,在25℃时的电动势为0.209V。
玻璃电极|H+(a)||SCE。
当缓冲溶液由待测试液代替时,测得的电动势为0.312V,计算待测试液的pH。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“当下列电池中的标准溶液是pH=5.21的缓冲溶液时,在25℃…”相关的问题
更多“当下列电池中的标准溶液是pH=5.21的缓冲溶液时,在25℃…”相关的问题
当下列电池中的溶液是pH=4.00的缓冲溶液时,在25℃测得电池的电动势为0.209V:玻璃电极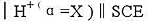 当缓冲溶液由未知溶液代替时,测得电池电动势如下:
当缓冲溶液由未知溶液代替时,测得电池电动势如下:
(a)0.312V; (b)0.088V; (c)-0.017V.试计算每种溶液的pH.
298K时测定下述电池的电动势:
玻璃电极|pH缓冲溶液|饱和甘汞电极
当所用缓冲溶液的pH=4.00时,测得电池的电动势为0.1120V。若换用另一缓冲溶液重测电动势,得E=0.3865V。试求该缓冲溶液的pH值。当电池中换用pH=2.50的缓冲溶液时,计算电池的电动势E。
A.不变
B.减缓
C.加快
D.无规律
在下列电池中Pt,H2(101.3kPa),HAc(xmol.L-1),Ac一(ymol.L-1)SCE当电池的电动势为0.620 V时,计算溶液中[HAe]和[NaAc]的比值为多少(25℃)?(已知E(SCE)=0.242 V,醋酸的pKa=4.74)
A.降低Fe3+/Fe2+电对的电位
B.控制反应时的PH值
C.消除Fe3+的颜色
D.降低溶液中Fe2+的浓度