 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在酸性介质中,以等浓度的K2Cr2O7溶液滴定20.00mL的Fe2+溶液,试推导其化学计量点时电势的计算公式.假设酸度的影响忽略不计,c(H+)=1.00mol·L-1.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在酸性介质中,以等浓度的K2Cr2O7溶液滴定20.00mL…”相关的问题
更多“在酸性介质中,以等浓度的K2Cr2O7溶液滴定20.00mL…”相关的问题
将只含KMnO4和K2Cr2O7的混合物0.2400g与过量KI在酸性介质中反应,析出的碘用0.2000mol·L-1Na2S2O3溶液滴定,耗去30.00mL。计算混合物中KMnO4的质量。
分别计算0.100mol/L KMnO4和0.100mol/L K2Cr2O7在H+浓度为1.0mol/L介质中还原一半时的电位。计算结果说明什么?已知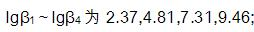 ,
,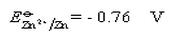
取一含KI和KBr的样品1.000g,溶解于水中并稀释至200.0mL,取其50.00mL,在中性介质中用Br2处理,以使I-变成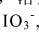 ,过量的Br2用沸腾法除去。再加入过量的KI溶液,酸化后,生成的I2用0.05000mol/L Na2S2O3溶液滴定,消耗40.80mL。另取50.00mL被测溶液,用K2Cr2O7强酸性溶液氧化,释放出来的I2和Br2被蒸馏出来,并收集在较浓的KI溶液中,再用Na2S2O3溶液滴定,消耗29.80mL,计算原样品中KI和KBr的含量。
,过量的Br2用沸腾法除去。再加入过量的KI溶液,酸化后,生成的I2用0.05000mol/L Na2S2O3溶液滴定,消耗40.80mL。另取50.00mL被测溶液,用K2Cr2O7强酸性溶液氧化,释放出来的I2和Br2被蒸馏出来,并收集在较浓的KI溶液中,再用Na2S2O3溶液滴定,消耗29.80mL,计算原样品中KI和KBr的含量。
化合物A分子式为C5H12O,A与K2Cr2O7/H2SO4反应生成化合物B。A脱水得到分子式为C5H10的化合物C,C与酸性KMnO4溶液反应生成化合物D和E,B和D均能发生碘仿反应。推测A、B、C、D、E的结构简式。
欲配制Na2C2O4标准溶液用于标定KMnO4溶液(在酸性介质中),已知c(KMnO4)≈0.100mol/L,若要使标定时两种溶液消耗的体积相近,问应配制多大浓度的Na2C2O4溶液?要配制100mL溶液,应称取Na2C2O4多少克?
A.以HCl标准溶液滴定某碱样,所用滴定管因未洗净,滴定时管内壁挂有液滴
B.以K2Cr2O7为基准物,用碘量法标定Na2S2O3溶液的浓度时,滴定速度过快,并过早读出滴定管读数
C.基准物在称量时吸湿了
D.以EDTA标准溶液滴定钙镁含量时,滴定速度过快
E.以失去部分结晶水的硼砂为基准物,标定盐酸溶液的浓度
在水溶液中SO2作为还原剂还原(a)KMnO4溶液到MnSO4;(b)K2Cr2O7的酸性溶液到Cr3+离子;(c)Hg(NO3)2水溶液到金属汞。写出这些反应的方程式。
某硅酸盐试样1.000g,用重量法测得Fe2O3和Al2O3的总量为0.5000g。将沉淀溶解在酸性溶液中,并将Fe3+还原为Fe2+,然后用0.03000mol/L K2Cr2O7溶液滴定,用去25.00mL。计算试样中FeO和Al2O3的质量分数。
用K2Cr2O7标准滴定溶液在c(HCl)=1mol/L HCl溶液中滴定Fe2+,反应达化学计量点时的电位是1.02V,求此时Fe3+与Fe2+的浓度比。
A.直接滴定法
B.返滴定法
C.置换滴定法
D.间接滴定法