 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算AgCl沉淀在pH=8.0,配位剂L的总浓度为0.10moL/L溶液中的溶解度。(AgCl的Ksp=10-9.74;HL的pKa=10;AgL2的lgβ1=3.0,lgβ2=7.0)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“计算AgCl沉淀在pH=8.0,配位剂L的总浓度为0.10m…”相关的问题
更多“计算AgCl沉淀在pH=8.0,配位剂L的总浓度为0.10m…”相关的问题
金属离子Fe2+、Cu2+、Al3+、Mn2+浓度均为0.01mol/L,计算各离子开始沉淀为氢氧化物和沉淀完全的pH。已知 =8.0×10-16,
=8.0×10-16, =2.6×10-19,
=2.6×10-19, =4.6×10-33,
=4.6×10-33, =1.9×10-13。
=1.9×10-13。
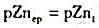 ),溶液的酸度应控制在多少?
),溶液的酸度应控制在多少?
计算pH=8.0和4.00mol/L HCl溶液中As(Ⅴ)/As(Ⅲ)电对的条件电位。(忽略离子强度的影响。)
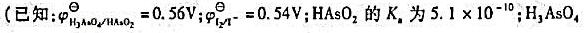
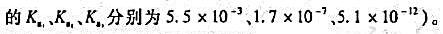 并判断pH=8.0和[H+]=5.0mol/L条件下,下列反应的方向:
并判断pH=8.0和[H+]=5.0mol/L条件下,下列反应的方向: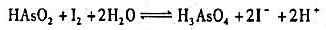 。
。
A.配位掩蔽剂必须可溶且无色
B.沉淀掩蔽剂的溶解度要很小
C.氧化还原掩蔽剂必须改变干扰离子的价态
D.掩蔽剂的用量越多越好
E.掩蔽剂最好是无毒的
在用配位滴定法连续测定溶液中的Al3+、Fe3+时,取50mL试液,用缓冲溶液控制其pH=2.0,以水杨酸为指示剂,用0.04016mol/L的EDTA标准溶液滴定,直到Fe3+-水杨酸配位化合物的红色刚刚消失,共用去EDTA标准溶液29.61mL。再准确称取50.00mL相同浓度的EDTA至溶液中,煮沸使Al3+完全配位,将pH调到5.0。此时用0.03228mol/L Fe3+标准溶液19.03mL返滴定剩余的EDTA,终点的颜色与上面曾出现的Fe3+-水杨酸配位化合物的红色一致。计算原试液中Al3+、Fe3+的浓度。
称取含有NaCl和NaBr的试样0.6280g,溶解后用AgNO3溶液处理,得到干燥的AgCl和AgBr沉淀0.5064g。另称取相同质量的试样1份,用0.1050mol/L AgNO3溶液滴定至终点,消耗28.34mL。计算试样中NaCl和NaBr的质量分数。
A.CaF2的溶解度在pH=3的溶液中较在pH=5的溶液中为大
B.BaSO4沉淀可用水洗涤,而AgCl沉淀要用稀HNO3洗涤
C.BaSO4沉淀和Fe2O3·nH2O沉淀都不宜陈化
D.ZnS会在HgS沉淀的表面上后沉淀
E.以上结果都不对