 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
(i)证明 并由此导出 其中与分别代表体积为V0时的定容热容与压强为p0时的定压热容,它们都只是温度
(i)证明
并由此导出
其中与
分别代表体积为V0时的定容热容与压强为p0时的定压热容,它们都只是温度的函数.
(ii)根据以上Cv,Cp两式证明,理想气体的Cv,与Cp只是温度的函数.
(iii)证明范德瓦耳斯气体的Cv只是温度的函数,与体积无关.
 答案
答案
证明:(i)由
(1)
对V求偏微商,得
(2)
以上第三个等式用到麦克斯韦关系
(3)
注意到Cv是两个独立变量的函数.若选(T,V)为独立变量,确定Cv(T,V)的一般做法是按下列公式
(4)
其中的积分是沿T-V状态空间中从(T0,V0)到(T,V)的任意路径完成的.比较简单的做法是把积分路径选成如下的两段直线:
(Ⅰ):(T0,V0)→(T,V0)(等容过程);
(Ⅱ):(T,V0)→(T,V) (等温过程).

则(4)式化为
令
(6)
其中积分是在固定体积V=V0下完成的(省去了(Ⅰ)的标记).利用(2),则(5)式可表为
(7)
上式中的积分是在固定温度为T下完成的(标记(Ⅱ)已省去).由(7)式可以看出,要确定任意(T,V)下的Cv(T,V),只需知道某固定体积V=V0下的定容热容(T)(注意它是T的函数),以及物态方程.这将使实验测量的工作量减少.
类似地,由
(8)
得
(9)
以上第三个等式用到麦克斯韦关系
(10)
选T-p空间时等压过程(p=p0)与等温过程为积分路径,最后可得
(11)
其中(T)代表保持压强固定为p0时的定压热容,它只是T的函数.第二项的积分是在保持温度固定为T下完成的.
注意公式(2),(7)以及(9),(11)对任何p-V-T系统均成立.
(ii)对理想气体,由物态方程
pV=NRT, (12)
当V固定时,p是T的线性函数;当p固定时,V是T的线性函数,
故有
(13)
(14)
由(2)与(9)式,得
(15)
(16)
亦即理想气体的Cv与Cp都只是温度的函数.
(iii)范德瓦耳斯气体的物态方程为
(17)
在V固定下,p是T的线性函数,故有
(18)
由公式(2),即得
(19)
表明范德瓦耳斯气体的Cv只是温度的函数,与体积无关.顺便指出,当V→∞时,范德瓦耳斯气体趋于理想气体.既然范德瓦耳斯气体的Cv与V无关,因而任意体积时的Cv与V→∞时的Cv相同.也就是说,范德瓦耳斯气体的Cv与理想气体的定容热容(记为)相等,即
(20)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案

 更多“(i)证明 并由此导出 其中与分别代表体积为V0时的定容热容…”相关的问题
更多“(i)证明 并由此导出 其中与分别代表体积为V0时的定容热容…”相关的问题

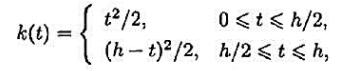
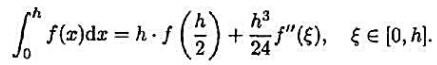
 ;由此导出压强P和体积弹性模量
;由此导出压强P和体积弹性模量 )的体积弹性模量值,并与杨氏模量的量级1011N/m2比较。
)的体积弹性模量值,并与杨氏模量的量级1011N/m2比较。
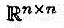 的三角分解,其中|lij|<1。并设aiT,uiT分别表示A和U的第i行,验证
的三角分解,其中|lij|<1。并设aiT,uiT分别表示A和U的第i行,验证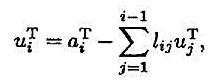 并证明
并证明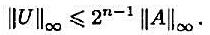
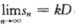 ,其中k=1/S称为增值率; (3)假设边际消费倾向为80%,试问此时k为多少?
,其中k=1/S称为增值率; (3)假设边际消费倾向为80%,试问此时k为多少?
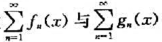 在区间I都一致收敛,则函数项级数
在区间I都一致收敛,则函数项级数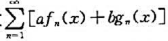 在区间I也一致收敛,其中a与b是常数.
在区间I也一致收敛,其中a与b是常数.
















