 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
元素观是化学的重要观念之一。下列有关元素的说法中错误的是()
A.元素是具有相同核电荷数的一类原子的总称
B.元素周期表,元素的原子序数等于其核电荷数
C.同种元素的原子核内质子数与中子数一定相等
D.在物质发生化学变化时,原子的种类不变,元素也不会改变
 答案
答案
C、同种元素的原子核内质子数与中子数一定相等
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.元素是具有相同核电荷数的一类原子的总称
B.元素周期表,元素的原子序数等于其核电荷数
C.同种元素的原子核内质子数与中子数一定相等
D.在物质发生化学变化时,原子的种类不变,元素也不会改变
 答案
答案
C、同种元素的原子核内质子数与中子数一定相等
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“元素观是化学的重要观念之一。下列有关元素的说法中错误的是()”相关的问题
更多“元素观是化学的重要观念之一。下列有关元素的说法中错误的是()”相关的问题
A.元素观:二氧化碳是由碳元素和氧元素组成的
B.微粒观:保持氧气化学性质的最小微粒是氧气分子
C.变化观:氢气在空气中燃烧生成水
D.守恒观:24g镁和32g氧气反应,一定生成54g氧化镁
A.元素观:金刚石和石墨均由碳元素组成
B.分类观:从组成上看干冰和酒精都属于氧化物
C.变化观:氢气和水可以相互转化
D.微粒观:一个一氧化碳分子由一个碳原子和一个氧原子构成
A.元素观: 金刚石和石墨均由碳元素组成
B.分类观:从组成上看二氧化碳和酒精(C2H6O)都属于氧化物
C.变化观: 氢气和水可以相互转化
D.微粒观: 一个一氧化碳分子由一个碳原子和一个氧原子构成
A.硫酸铜、食盐、纯碱- -盐
B.硫酸铵、硝酸钾、尿素--氮肥
C.空气、石油、碘酒--混合物
D.硫元素、氧元素、氮元素--非金属元素
A.元素周期表揭示了化学元素间的内在联系,是化学发展史上的重要里程碑之一
B.元素周期表中,总共有18个纵行,16个族,过渡元素都为副族元素
C.在周期表中,第ⅡA族元素都为金属元素
D.X3+的核外电子数目为10,则X在第三周期第ⅢA族
阅读下列素材。回答有关问题:
1868年,化学家迈尔研究已知元素的原子量与其物理性质的关系时。把性质相近的元素划分为一个族.并与l869年制作了他的第一张元素周期表。
1869年,化学家门捷列夫研究元素原子量与元素化学性质的关系时,把63种元素排列成几行。同年,他公布了他的第一张元素周期表,后来他汲取了迈尔周期表的优点,进行了更详细的族的划分】分,并于1871年公布了他的第二张元素周期表。
之后。元素周期表被不断完善。成为化学研究的重要工具,到20世纪初,物理学家们逐步
揭开了原子结构的秘密.人们才逐渐清楚了元素的性质呈周期性变化的原因。问题:
(1)迈尔和门捷列夫进行“族”划分时,运用的是什么科学方法?他们在研究元素原子量与性质的关系时不同之处是什么?
(2)元素周期律的发现对化学科学发展有什么重要意义?(3)举例说明元素周期律对化学知识学习的指导作用。
A.轮作在提高对矿质元素利用率的同时,可改变原有的食物链,从而增产
B.喷洒农药防治稻田害虫,目的是调整能量流动的关系,使能量流向对人类更有益的方向
C.锄地(松土)能降低土壤微生物的呼吸强度,减少二氧化碳排放,避免温室效应
阅读下列三段材料,按要求完成任务。
材料一《义务教育化学课程标准(2011年版)》关于元素的内容标准:认识氢、碳、氧、氮等与人类关系密切的常见元素,记住并能正确书写一些常见元素的名称和符号,知道元素的简单分类,形成“化学变化过程中元素不变”的观念。
材料二教科书的知识结构体系
绪言化学使世界变得更加绚丽多彩
第一单元走进化学世界
第二单元我们周围的空气
第三单元物质构成的奥秘
课题1分子和原子
课题2原子的结构
课题3元素
第四单元自然界的水
第五单元化学方程式
第六单元碳和碳的氧化物
第七单元燃料及其利用
第八单元金属和金属材料
第九单元溶液
第十单元酸和碱
第十一单元盐化肥
第十二单元化学与生活
材料三某版本教科书“元素”所呈现的部分内容:
一、元素
利用化学方法分析众多的物质.发现组成它们的基本成分——元素其实只有一百多种,就像可拼写出数十万个英文单词的字母只有26个一样。例如,蛋壳、贝壳和石灰石的主要成分都是碳酸钙,而碳酸钙是由碳、氧、钙这三种元素组成的。再如,氧气(02)、二氧化碳(C02)的组成和性质不同.但它们都含有氧元素。
氧分子和二氧化碳分子中都含有氧原子.这些氧原子的原子核内都含有8个质子,即核电荷数为8,化学上将质子数(即核电荷数)为8的所有氧原子统称为氧元素。同样,将质子数为1的所有氢原子统称为氢元素.将质子数为6的所有碳原子统称为碳元素。可见,元素是质子数(即核电荷数)相同的一类原子的总称。
在物质发生化学变化时。原子的种类不变.元素也不会改变。
【讨论】
在下列化学反应中.反应物与生成物相比较,分子是否发生了变化?原子是否发生了变化?
元素是否发生了变化?

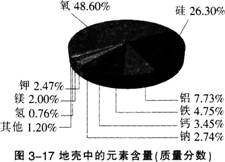
各种元素在地壳里的含量如图3—17所示,其中含量最多的是氧元素,它的质量分数接近50%,其次是硅元素。
自然界中,由一百多种元素组成的几千万种物质都是由原子、分子或离子构成的(如图3-18)。元素的化学性质与其原子的核外电子结构排布,特别是最外层电子的数目有关。

要求:
(1)试对本课内容进行学情分析。
(2)确定本课的三维教学目标。
(3)确定本课的教学重点和难点。
(4)设计本课教学内容的教学过程。
(5)对本课教学内容进行板书设计。
A.阳离子一定带正电荷,所以带有正电荷的粒子一定是阳离子
B.化合物是由不同种元素组成的纯净物,所以只含一种元素的物质一定不是化合物
C.氧化物中一定含有氧元素,所以含有氧元素的化合物一定是氧化物
D.同种元素的粒子具有相同的质子数,所以具有相同质子数的粒子一定属同一种元素