 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在25℃时,用Cu2+选择性电极作正极,饱和甘汞电极作负极组成工作电池,以测定Cu2+浓度。于100.00 mL含
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在25℃时,用Cu2+选择性电极作正极,饱和甘汞电极作负极组…”相关的问题
更多“在25℃时,用Cu2+选择性电极作正极,饱和甘汞电极作负极组…”相关的问题
用Cl-选择性电极作负极,饱和甘汞电极作正极组成电池测定某溶液中氯化物含量。取100mL此溶液在25℃时测得电池电动势为28.8mV。加入1.00mL浓度为0.475mol·L-1的经酸化的NaCl标准溶液后,测得电池电动势为53.5mV。求该溶液中氯化物浓度。
25℃时,用Ca2+选择性电极(负极)与饱和甘汞电极(正极)组成电池。在100mL Ca2+试液中,测得电动势为-0.415V。加入2mL浓度为0.218mol·L-1的Ca2+标准溶液后,测得电动势为-0.430V。求试液中的pCa。
用标准甘汞电极作正极,氢电极作负极(pH2=100kPa)与待测的HCl溶液组成电池。在25℃时,测得E=0.342V。当待测溶液为NaOH溶液时,测得E=1.050V。取此NaOH溶液20.00mL,用上述HCl溶液中和完全,需用HCl溶液多少毫升?
,测得E=1.050V,取此NaOH溶液20.00cm3,需上述HCl溶液多少立方厘米时才能完全中和? (已知25℃时,标准甘汞电极的电极电势为0.2828V,p(H2)=105Pa)
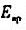 =0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。
=0.82V。假设滴定过程中体积不变,求该有机酸的摩尔质量。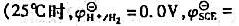
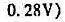
以SCE为正极,选择性电极作负极,放入0.001mol·L-1的F-溶液中时,测得E=-0.159V。当换用了含F-试液后,测得E=-0.212V。计算试液中F的浓度。
,它和标准氢电极(作正极)组成原电池,测得其电动势E=0.030V.[已知φθ(Cu2+/Cu)=0.342V]
(1)写出电池反应和原电池符号.
(2)计算[Cu(NH2)4]2+的稳定常数KIθ.
称取2.000 g一元酸HA(相对分子质量为120)溶于50.00 mL水中,用0.200 0 mol.L-1NaOH溶液滴定,用标准甘汞电极(NCE)作正极,氢电极作负极,当酸被中和一半时,在30℃下测得E=0.583 V,完全中和时,E=0.823 V,计算试样中HA的质量分数。(30℃时RT/F=0.060)
A.纯铜作阳极,含Zn和Ag的铜合金作阴极
B.含Zn和Ag的铜合金作阳极,纯铜作阴极
C.用纯铁作阳极,纯铜作阴极
D.用石墨作阳极,纯铜作阴极