 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
已知H3PO4浓度为HCl浓度的1/2,以酚酞为指示剂,用同一NaOH溶液滴定H3PO4和HCl溶液,消耗的NaOH体积分别为V1与V2,则V1与V2的关系为( )。
A.V1=V2
B.V1>V2
C.V1<V2
D.V1=2V2
E.V2=2V1
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.V1=V2
B.V1>V2
C.V1<V2
D.V1=2V2
E.V2=2V1
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知H3PO4浓度为HCl浓度的1/2,以酚酞为指示剂,用同…”相关的问题
更多“已知H3PO4浓度为HCl浓度的1/2,以酚酞为指示剂,用同…”相关的问题
A.#图片0$#
B.#图片1$#
C.#图片2$#
D.#图片3$#
为测定HCl与H3PO4混合溶液中各钼分的浓度,取两份此试液。每份25.00mL,分别用0.2500mol·L-1NaOH标准溶液滴定,第一份用甲基橙为指示剂,消耗30.00mLNaOH标准溶液,第二份用酚酞为指示剂,消耗40.00mL。溶液中HCl与H3PO4的浓度关系是
A.C(H3P04)=c(HCl) B.c(H3PO4)=2c(HCl)
C.2c(H3PO4)=c(HCl)
某溶液中可能含下列物质的某些成分:H3PO4,NaH2PO4,Na2HPO4,HCl,取该溶液25.00cm3,甲基橙为指示剂,终点时用去0.2500mol·dm-3。NaOH溶液31.20cm3。另取25.00cm3试液,以酚酞为指示剂,终点时用去上述NaOH溶液42.34cm3。问该溶液含上述哪几种成分?浓度各为多少?
(1)计算pH=5.0时,H3PO4的分布系数δ3、δ2、δ1、δ0。(2)假定H3PO4各种形式的总浓度是0.050mol/L,问此时H3PO4,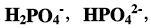
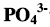 的浓度各为多少?
的浓度各为多少?
称取碳酸钠基准物0.2018g,用甲基橙为指示剂,滴定消耗HCl标准溶液30.55mL,计算HCl标准溶液的浓度。已知M(Na2CO3)=106.0g/mol。
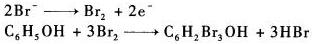 电流强度为8.50 mA,到达终点所需时间250 s,试计算试液中苯酚的浓度为多少?(以mg?L-1为单位,已知M(苯酚)=94.1 1 g?mol-1)
电流强度为8.50 mA,到达终点所需时间250 s,试计算试液中苯酚的浓度为多少?(以mg?L-1为单位,已知M(苯酚)=94.1 1 g?mol-1)