 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用0.1224mol/L HCl滴定可能含有NaOH、Na2CO3、NaHCO3的溶液,滴至酚酞终点消耗34.66mL。若滴至溴甲酚绿终点,消
用0.1224mol/L HCl滴定可能含有NaOH、Na2CO3、NaHCO3的溶液,滴至酚酞终点消耗34.66mL。若滴至溴甲酚绿终点,消耗41.24mL,判断溶液的组成,并计算各组分的质量。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用0.1224mol/L HCl滴定可能含有NaOH、Na2CO3、NaHCO3的溶液,滴至酚酞终点消耗34.66mL。若滴至溴甲酚绿终点,消耗41.24mL,判断溶液的组成,并计算各组分的质量。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“用0.1224mol/L HCl滴定可能含有NaOH、Na2…”相关的问题
更多“用0.1224mol/L HCl滴定可能含有NaOH、Na2…”相关的问题
在0.1mol/L HCl溶液中,用Fe3+滴定Sn2+,其反应为
2Fe3++Sn2+====2Fe2++Sn4+
将0.2497g CaO试样溶于25.00mL c(HCl)=0.2803mol/L的HCl溶液中,剩余酸用c(NaOH)=0.2786mol/L的NaOH标准滴定溶液返滴定,消耗11.64mL,求试样中CaO的质量分数。
已知H3PO4的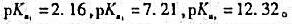 若用0.10mol/L的HCl溶液滴定0.10mol/L的Na3PO4溶液,则滴定到第二个化学计量点时体系的pH=()。
若用0.10mol/L的HCl溶液滴定0.10mol/L的Na3PO4溶液,则滴定到第二个化学计量点时体系的pH=()。
用K2Cr2O7标准滴定溶液在c(HCl)=1mol/L HCl溶液中滴定Fe2+,反应达化学计量点时的电位是1.02V,求此时Fe3+与Fe2+的浓度比。
称取混合碱样品0.6839g,以酚酞为指示剂,用c(HCl)=0.2000mol/L HCl标准滴定溶液滴定至终点,用去HCl溶液23.10mL,再加甲基橙指示剂,继续滴定至终点,又消耗HCl溶液26.81mL,求混合碱的组成及各组分的含量。
在1mol/L HCl溶液中,用Fe3+滴定Sn2-,计算下列滴定百分数时的电位:9%、50%、91%、99%、99.9%、100%、100.1%、101%、110%、200%。
用0.5000mol/L的HCl溶液滴定0.5000mol/L一元弱碱B(pKb=6.00),计算化学计量点的pH和滴定突跃范围。若所用溶液的浓度都是0.0200mol/L,结果又如何?
A.甲基橙
B.甲基红
C.酚酞
D.二甲酚橙
有一含Na2CO3与NaOH的混合物。现称取试样0.5895g,溶于水中,用0.3000mol/L HCI滴定至酚酞变色时,用去HCl 24.08mL;加甲基橙后继续用HCl滴定,又消耗HCl 12.02mL。试计算试样中Na2CO3与NaOH的质量分数。
某试样含有Na2CO3、NaHCO3及其他惰性物质。称取试样0.3010g,用酚酞作指示剂滴定,用去0.1060mol/L的HCl溶液20.10mL,继续用甲基橙作指示剂滴定,共用去HCl 47.70mL,计算试样中Na2CO3与NaHCO3的质量分数。