 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
若电极反应Cu2++2e====Cu的电极电势为E1,则2Cu2++4e====2Cu的电极电势为2E1;
若电极反应Cu2++2e====Cu的电极电势为E1,则2Cu2++4e====2Cu的电极电势为2E1;
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
若电极反应Cu2++2e====Cu的电极电势为E1,则2Cu2++4e====2Cu的电极电势为2E1;
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“若电极反应Cu2++2e====Cu的电极电势为E1,则2C…”相关的问题
更多“若电极反应Cu2++2e====Cu的电极电势为E1,则2C…”相关的问题
已知电极反应Cu2++2e====Cu的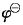 为0.34V,则电极反应:2Cu-4e====2Cu2+的
为0.34V,则电极反应:2Cu-4e====2Cu2+的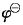 值为( )。
值为( )。
(A) -0.68V (B) +0.68V (C) -0.34V (D) 0.34V
A.E1-E2
B.E1-2E2
C.E2-E1
D.2E2-E1
已知电极反应:Cu++e-=Cu的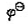 (Cu+/Cu)=0.52V,CuCl的
(Cu+/Cu)=0.52V,CuCl的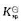 =1.7X10-7。求电极反应CuCl+e-=Cu+CI-的标准电极电势。
=1.7X10-7。求电极反应CuCl+e-=Cu+CI-的标准电极电势。
写出以下电池的电极反应、电池反应方程式,并计算电池电动热.
(1)Zn|Zn2+(1×10-6mol·dm-3)||Cu2+(0.01mol·dm-3)|Cu
(2)Cu|Cu2+(0.01mol·dm-3)||Cu2+(2.0mol·dm-3)|Cu
(3)Pt,H2(1×105Pa)|HAc(0.1mol·dm-3)KCl(饱和),Hg2Cl2|Hg
已知Eθ(MnO-4/Mn2+)=1.51V,Eθ(Cl2/Cl-)=1.36V,若将此两电对组成原电池,请写出:
(1)该电池的电池符号;
(2)写出正负电极的电极反应和电池反应以及电池标准电动势;
(3)计算电池反应在25℃时和Kθ;
(4)当[H+] = 1.0×10-2mol•L-1,而其他离子浓度均为1.0 mol•L-1,= 100 kPa时的电池电动势.
A.
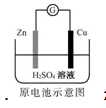 Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
B.
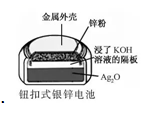 正极的电极反应式为Ag2O+2e−+H22Ag+2OH−
正极的电极反应式为Ag2O+2e−+H22Ag+2OH−
C.
 锌筒作负极,发生氧化反应,锌筒会变薄
锌筒作负极,发生氧化反应,锌筒会变薄
D.
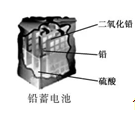 使用一段时间后,电解质溶液的酸性减弱,导电能力下降
使用一段时间后,电解质溶液的酸性减弱,导电能力下降
将如图所示实验装置的K闭合(已知:盐桥中装有琼脂凝胶,内含KCl),下列判断正确的是()。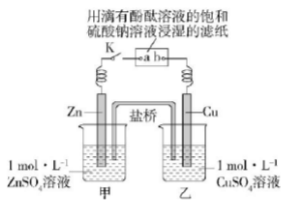
A.Cu电极上发生还原反应
B.电子沿Zn→a→b→Cu路径移动
C.片刻后甲池中c(SO42-)增大
D.片刻后可观察到滤纸b处变红色
试写出下列各电池的电极反应和电池反应。 (1)Cu(s)|CuSO4(a1)||AgNO3(a2)|Ag(s) (2)Pb(s)|PbSO4(s)|K2SO4(a1)||HCl(a2)|AgCl(s)|Ag(s) (3)Pt|H2(P)|NaOH(a)|HgO(s)|Hg(1) (4)Pt|H2(P1)|H2SO4(m)|H2(P2)|Pt (5)K(Hg)(a1)|K+(a2)||Cl-(a3)|Hg2Cl2(s)|Hg(1)