题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
生产、合成与制备。(1)以N2和H2为主要原料制备NH4NO3。(2)由NH3制备N2H≇
生产、合成与制备。
(1)以N2和H2为主要原料制备NH4NO3。
(2)由NH3制备N2H4和HN3。
(3)由NaNO3制备N2O5。
(4)以磷酸钙矿为主要原料生产P2O5和单质P。
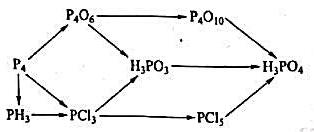
(5)完成下列物质转化的化学反应方程式并给出反应条件。
(6)以As2S3为主要原料制备As2O3和H3AsO4。
(7)由Sb2S3矿生产单质Sb。
(8)由Bi2S3制备NaBiO3。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“生产、合成与制备。(1)以N2和H2为主要原料制备NH4NO…”相关的问题
更多“生产、合成与制备。(1)以N2和H2为主要原料制备NH4NO…”相关的问题
 CH4(g)的A,Gf=19290/mol.现有与碳反应的气体,其中含有CH.(g)10%,H2(g)80%,N2(g)10%(体积%)。试问:
CH4(g)的A,Gf=19290/mol.现有与碳反应的气体,其中含有CH.(g)10%,H2(g)80%,N2(g)10%(体积%)。试问: