 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某溶液中含有Fe2+和Fe3+,浓度均为0.10mol·dm-3,若要求沉淀完全是Fe(OH)3
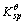 =2.8×10-39,Fe(OH)2的
=2.8×10-39,Fe(OH)2的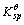 =4.9×10-17。
=4.9×10-17。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
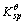 =2.8×10-39,Fe(OH)2的
=2.8×10-39,Fe(OH)2的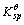 =4.9×10-17。
=4.9×10-17。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某溶液中含有Fe2+和Fe3+,浓度均为0.10mol·dm…”相关的问题
更多“某溶液中含有Fe2+和Fe3+,浓度均为0.10mol·dm…”相关的问题
测定某试液中Fe2+、Fe3+的含量。吸取25.00mL该试液,在pH=10时用浓度为0.01500mol/L的EDTA标准溶液滴定,耗用15.40mL,调至pH=6,继续滴定,又耗用溶液体积14.10mL,计算两者的浓度(以mg/mL表示)。
已知

于0.100mol/LFe3+和0.250mol/LHCl混合溶液中,通入H2S气体使之达到平衡,求此时溶液中Fe3+的浓度。已知H2S饱和溶液的浓度为0.100mol/L;φ0(S/H2S)=0.141V;φ0(Fe3+/Fe2+)=0.71V。
A.2.81~6.86
B.1.81~ 3.14
C.3.14~6.92
D.1.81~ 6.92
用K2Cr2O7标准滴定溶液在c(HCl)=1mol/L HCl溶液中滴定Fe2+,反应达化学计量点时的电位是1.02V,求此时Fe3+与Fe2+的浓度比。
某硅酸盐试样1.000g,用重量法测得Fe2O3和Al2O3的总量为0.5000g。将沉淀溶解在酸性溶液中,并将Fe3+还原为Fe2+,然后用0.03000mol/L K2Cr2O7溶液滴定,用去25.00mL。计算试样中FeO和Al2O3的质量分数。
某溶液中含有Ca2+、Ba2+,其浓度均为0.1mol·L-1,缓慢加入Na2SO4,开始生成的是何沉淀?开始沉淀时
某溶液中含有Ca2+、Ba2+,其浓度均为0.1mol·L-1,缓慢加入Na2SO4,开始生成的是何沉淀?开始沉淀时
 (AgCl)=1.8×10-10,
(AgCl)=1.8×10-10, (Ag2CO3)=8.45×10-12,
(Ag2CO3)=8.45×10-12, (AgI)=8.5×10-17。某溶液中含有浓度c均为0.1mol·L-1的Cl-、
(AgI)=8.5×10-17。某溶液中含有浓度c均为0.1mol·L-1的Cl-、 、I-,若往此溶液中逐滴加入AgNO3溶液,产生沉淀的先后次序是:
、I-,若往此溶液中逐滴加入AgNO3溶液,产生沉淀的先后次序是:A.AgI、Ag2CO3、AgCl;
B.Ag2CO3、AgI、AgCl;
C.AgCl、Ag2CO3、AgI;
D.AgI、AgCl、Ag2CO3。
A.(Fe3+/Fe2+)
B.(Fe3+/Fe2+)+
C.(Fe3+/Fe2+)+0.05916V
D.(Fe3+/Fe2+)-0.05916V
 +6Fe2++14H+→2Cr3++6Fe3++7H2O中,达到化学计量点时,下列各种说法正确的是( )。
+6Fe2++14H+→2Cr3++6Fe3++7H2O中,达到化学计量点时,下列各种说法正确的是( )。A.溶液中c(Fe3+)与c(Cr3+)相等
B.溶液中不存在Fe2+和
C.溶液中两个电对Fe3+/Fe2+和
D.溶液中两个电对Fe3+/Fe2+和