 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在用Na2C2O4标定KMnO4的实验中(1)溶液酸度为何要在1mol/L左右?若酸度较低有何影响?为何要在H2SO4介质中,而不能在HCl或HNO3介质中进行滴定?(2)为何必须用KMnO4滴定Na2C2O4而不能以Na2C2O4滴定KMnO4?(3)为何要在加热70~80℃下进行,且开始必须慢滴?
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在用Na2C2O4标定KMnO4的实验中(1)溶液酸度为何要…”相关的问题
更多“在用Na2C2O4标定KMnO4的实验中(1)溶液酸度为何要…”相关的问题
欲配制Na2C2O4标准溶液用于标定KMnO4溶液(在酸性介质中),已知c(KMnO4)≈0.100mol/L,若要使标定时两种溶液消耗的体积相近,问应配制多大浓度的Na2C2O4溶液?要配制100mL溶液,应称取Na2C2O4多少克?
用Na2C2O4标定KMnO4的浓度,满足式( )。
A.n(KMnO4)=5n(Na2C2O4) B.n(KMnO4)=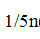 (Na2C2O4)
(Na2C2O4)
C.n(KMnO4)=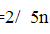 (Na2C2O4)D.n(KMnO4)=
(Na2C2O4)D.n(KMnO4)=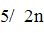 (Na2C2O4)
(Na2C2O4)
称取基准物质Na2C2O40.1000g,标定KMn04溶液时用去24.85mL,计算KMnO4溶液的浓度c(KMnO4)为多少?
溶液的酸度越高,KMnO4氧化Na2C2O4的反应进行得越完全,所以用基准Na2C2O4标定KMnO4溶液时,溶液的酸度越高越好。( )
用Na2C2O4标定KMnO4溶液时,Na2C2O4溶液要在75~85℃滴定,温度低了则______;温度高了则______。
A.H2C2O4挥发
B.H2C2O4分解
C.H2C2O4析出
D.H2C2O4与空气中的氧反应
E.H2C2O4脱水成酸酐