 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
钠原子的价电子结构为(3 s)1,第一激发态的电子结构为(3p)1,写出其光谱项符号。用光谱项符号表示钠
钠原子的价电子结构为(3 s)1,第一激发态的电子结构为(3p)1,写出其光谱项符号。用光谱项符号表示钠原子的589.0nm和589.6 nm的两条谱线。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
钠原子的价电子结构为(3 s)1,第一激发态的电子结构为(3p)1,写出其光谱项符号。用光谱项符号表示钠原子的589.0nm和589.6 nm的两条谱线。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“钠原子的价电子结构为(3 s)1,第一激发态的电子结构为(3…”相关的问题
更多“钠原子的价电子结构为(3 s)1,第一激发态的电子结构为(3…”相关的问题
VA族元素氮、磷、砷(As)、锑(Sb)、铋(Bi)的单质及其化合物在科研和生产中有许多重要用途。
(1)铋合金可用于自动喷水器的安全塞,一旦发生火灾时,安全塞会“自动”熔化,喷出水来灭火。铋的价电子排布式为()。
(2)第三周期元素中第一电离能大于磷的元素有()(填元素符号)。
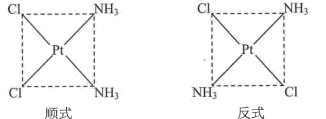
(3)Pt(NH3)2C12具有如图所示的两种平面四边形结构(一种有抗癌作用),其中在水中的溶解度较小是()(填“顺式”或“反式”)。
 (4)氨硼烷(BH3▪NH3)是一种储氢材料,与乙烷互为等电子体,熔点为104℃。氨硼烷晶体中各种微粒间的作用力涉及()(填标号)。
(4)氨硼烷(BH3▪NH3)是一种储氢材料,与乙烷互为等电子体,熔点为104℃。氨硼烷晶体中各种微粒间的作用力涉及()(填标号)。
A.范德华力B.离子键C.配位键D.金属键
(5)偏亚砷酸钠(NaAsO2)是一种灭生性除草剂,可杀死各种草本植物,其阴离子的立体构型为()。
(6)化肥厂生产的(NH4)2SO4中往往含有少量极易被植物根系吸收的具有正四面体结构的N4H44+,其结构式为(),其中N原子的杂化方式为()。
(7)镧、铁、锑三种元素组成的一种固体能实现热电效应。该固体晶胞结构如图l所示,晶胞参数为anm,Fe原子填在6个Sb原子形成的正八面体空隙中,晶胞6个表面的结构都如图2所示。
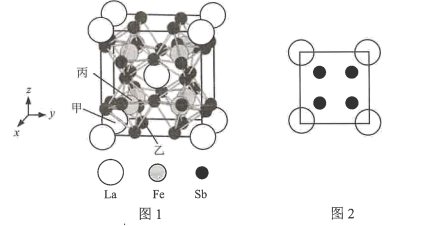 ①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图l中原子甲的坐标为(0,0,0),原子乙的坐标为(1/4,1/4,0),则原子丙的坐标为()。
①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图l中原子甲的坐标为(0,0,0),原子乙的坐标为(1/4,1/4,0),则原子丙的坐标为()。
②设阿伏加德罗常数的值为NA,则该固体的密度ρ=()g·cm-3(列出计算式即可)。
A.e原子的价电子排布式为3d64s2
B.基态S原子的轨道表示式为
C.基态Cu原子核外电子共有15种不同的运动状态
D.4f、4s、3d原子轨道的能量关系为:E(4f)>E(4s)>E(3d)
A.3p能级有一个空轨道的基态原子和核外电子排布为1s22s22p63s23p2的原子
B.2p能级有一个未成对电子的基态原子和价电子排布为2s22p5的原子
C.M层全充满而N层4s2的原子和核外电子排布为1s22s22p63s23p63d24s2的原子
D.最外层电子数是核外电子总数的1/5的原子和价电子排布为4s24p3的原子
A.q \f(k,2)
B.k
C.q \f(3k,2)
D.2k
给出符合下列条件元素的元素符号和价电子构型:
(1)最高能级组中的d轨道和s轨道均半充满的元素:
(2)角量子数l=3的轨道半充满的非放射性元素;
(3)M和M+的价层d轨道电子数不同的元素;
(4)主量子数n=6且角量子数l=0的轨道与l=1的轨道中电子数相等的元素。
A.氮原子价电子的P电子成分比例越大,碱性越强
B.氮原子附近有吸电子基团则使碱性增强
C.氮原子处于酰胺状态则碱性极弱
D.生物碱的立体结构有利于氮原子接受质子,则其碱性性增强
E.氮原子附近取代基团不利于其共轭酸中的质子形成氢键缔合,则碱性强