 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
试根据汞的元素电势图回答问题:①在酸性介质中Hg22+能否发生歧化反应?②计算反应的平
试根据汞的元素电势图回答问题:
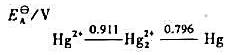
①在酸性介质中Hg22+能否发生歧化反应?
②计算反应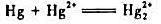 的平衡常数Kθ;
的平衡常数Kθ;
③拟使Hg(I)歧化为Hg(II)和Hg,应该怎样做?试举两个实例加以说明。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
试根据汞的元素电势图回答问题:
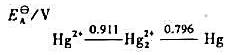
①在酸性介质中Hg22+能否发生歧化反应?
②计算反应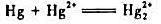 的平衡常数Kθ;
的平衡常数Kθ;
③拟使Hg(I)歧化为Hg(II)和Hg,应该怎样做?试举两个实例加以说明。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“试根据汞的元素电势图回答问题:①在酸性介质中Hg22+能否发…”相关的问题
更多“试根据汞的元素电势图回答问题:①在酸性介质中Hg22+能否发…”相关的问题
由附表六中查出酸性溶液中
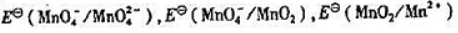
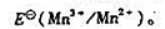
(1)颐出锰元素在酸性溶液中的元素电势图;
(2)计算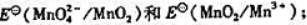
(3)MnO42-能否歧化?写出相应的反应方程式,并计算该反应的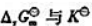 还有哪些物质能歧化?
还有哪些物质能歧化?
(4)计算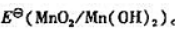
已知以下标准电极电势:

①画出酸性介质中铀的元素电势图;
②预测哪个氧化态最稳定;
③预测哪些氧化态会发生歧化反应;
④哪些氧化态在空气中不稳定?
(1)写出下列各电对的电极反应式,并根据元素电势图给出各电极反应的标准电极电势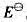 。
。
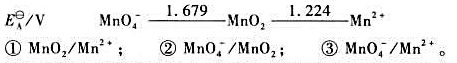
(2)试写出以电对①为负极、电对②为正极的原电池的电池反应,并计算原电池的标准电动势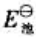 和电池反应的
和电池反应的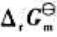 。
。
(3)试写出以电对①为负极、电对③为正极的原电池的电池反应,并计算原电池的标准电动势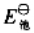 和电池反应的
和电池反应的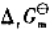 。
。
在图2.3所示的各图中,TM、TL、n均为实际方向,试回答各问题:
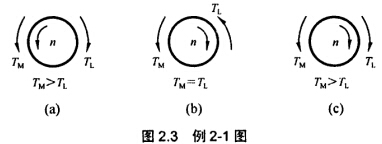
根据图示TM、TL、n的方向,列出各机电传动系统的运动方程式:
根据教材附表一中的相关数据主考虑电势图N2-HN4+,(aq)-NH;(aq)在酸性溶液中Eθ(N2/HN3)和Eθ(HN3/NH4+).写出HN3(aq)的岐化反应方程,计算25℃下该反应的标准平衡常数Kθ并评价NH3(aq)的稳定性.
如附图所示是碳的相图,试根据该图回答下列问题:
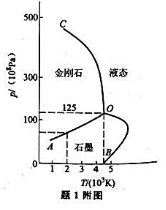
(1)说明曲线OA,OB,OC分别代表什么?
(2)说明点O的含义:
(3)碳在室温及101.325kPa下,以什么状态稳定存在?
(4)在2000K时,增加压力,使石墨转变成金刚石是一个放热反应,试从相图判断两者的摩尔体积Vm哪个大?
(5)从图上估计2000K时,将石墨变为金刚石需要多大压力?
图2—1、2—2、2—3是一项实验的三种可能结果。试根据图示的结果,回答下列问题: (1)该实验的目的是什么? (2)该实验有几个自变量?每个自变量各有几个水平?因变量是什么? (3)请用文字分别描述这三种可能的结果。
