 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
计算在1moL/LHClO4溶液中,用0.0200mol/LFe2+溶液还原等浓度的K2Cr2O7至
一半时的电位。(已知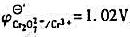 )
)
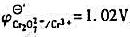 )
)
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
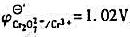 )
)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“计算在1moL/LHClO4溶液中,用0.0200mol/L…”相关的问题
更多“计算在1moL/LHClO4溶液中,用0.0200mol/L…”相关的问题
计算在溶液中c(

计算在1moldm-3NH3·H2O溶液体系中,当 1.00×10mol*-3dm-3时的
1.00×10mol*-3dm-3时的 为多少?[已知
为多少?[已知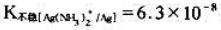 ]
]
在HgCl2=HgCl++Cl-体系中,已知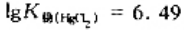 ,请计算在0.01mol·dm-3升汞溶液中的电离度及[HgCl+]/[HgCl2]的比值.
,请计算在0.01mol·dm-3升汞溶液中的电离度及[HgCl+]/[HgCl2]的比值.

 ,试计算在c(H+)=1.0mol/L,c(
,试计算在c(H+)=1.0mol/L,c(


某阳离子M2+可形成[MCl4]2-配离子,其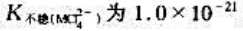 ,MI2的Ksp为1.0×10-15,请计算在1L溶液中,欲使0.010molMI2溶解,需Cl-的摩尔量.
,MI2的Ksp为1.0×10-15,请计算在1L溶液中,欲使0.010molMI2溶解,需Cl-的摩尔量.
用K2Cr2O7标准滴定溶液在c(HCl)=1mol/L HCl溶液中滴定Fe2+,反应达化学计量点时的电位是1.02V,求此时Fe3+与Fe2+的浓度比。
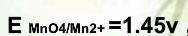 ,
,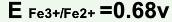 ,在此条件下用KMnO4标准溶液滴定Fe2+,其化学计量点时电位值是( )。
,在此条件下用KMnO4标准溶液滴定Fe2+,其化学计量点时电位值是( )。A.0.77V
B.1.06V
C.1.32V
D.1.45V