 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
溶解固体量是指将一定量的水样,用一定的过滤器过滤后所得到的澄清水,在105-110℃下蒸干后所残留的固体量。()
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“溶解固体量是指将一定量的水样,用一定的过滤器过滤后所得到的澄…”相关的问题
更多“溶解固体量是指将一定量的水样,用一定的过滤器过滤后所得到的澄…”相关的问题
A.饱和度
B.溶解度
C.溶解速度
D.溶解率
A.0.44um
B.0.45um
C.0.55um
D.0.46um
,将悬浮物、过滤膜和称量瓶经烘干、冷却至室温,称量至恒重,称得重量为45.2188g试计算水样中悬浮物的浓度。
称取土样1.000g溶解,将其中的磷沉淀为磷钼酸铵,用20.00mL0.1000mol·L-1
NaOH溶解沉淀,过量的NaOH用0.2000mol·L-1HNO37.50mL滴至酚酞终点,计算土样中w(P)、w(P2O5).已知
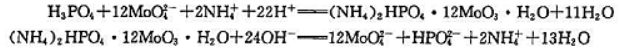
A.将显像剂结晶粉溶解于水中制成
B.为调整显像剂粘度,使显像剂不太浓,应加一定量的稀释剂
C.显像灵敏度高,挥发快,形成的显示扩散小
D.显示轮廓清晰,常与着色渗透液配合使用
A.在一定时间内机体呼出的二氧化碳量与氧摄入量的比值
B.在一定时间内机体氧摄入量与呼出的二氧化碳量的比值
C.呼出气体量与吸入气体量的比值
D.机体二氧化碳产生量与吸入气体总量的比值
【题目描述】
18.(10分)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。与Cl2相比ClO2不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
(1)在ClO2的制备方法中,有下列两种制备方法:
方法一:2NaClO3+4HCl===2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4===2ClO2↑+Na2SO4+O2↑+2H2O

用方法二制备的ClO2更适合用于饮用水的消毒,其主要原因是▲。
(2)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子的含量应不超过0.2mg·L-1。
饮用水中CIO2、CIO2的含量可用连续碘量法进行测定。CIO2被I-还原为CIO-2、Cl-的转化率与溶液pH的关系如右图所示。当pH≤2.0时,CIO-2也能被I-完全还原成Cl-。反应生成的I2用标准Na2S2O3溶液滴定: ①请写出pH≤2.0时,CIO-2与I-反应的离子议程式▲。 ②请完成相应的实验步骤: 步骤1:准确量取V mL水样加入到锥形瓶中。 步骤2:调节水样的pH为7.0~8.0。 步骤3:加入足量的KI晶体。 步骤4:加少量淀粉溶液,用c mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V1mL。 步骤5:▲。 ③根据上述分析数据,测得该饮用水样中CIO-2的浓度为▲mol·L-1(用含字母的代数式表示。) ④若饮用水中ClO-2的含量超标,可向其中加入适量的Fe2+将ClO-2还原成Cl-, 该反应的氧化产物是▲(填化学式)。
(1)方法二制备的ClO2中不含Cl2
