 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
加入NaOH和Na2CO3溶液后,Ca2+,Mg2+,Ba2+离子分别生成CaCO3,Mg(OH)2和BaCO3沉淀。()
此题为判断题(对,错)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
此题为判断题(对,错)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“加入NaOH和Na2CO3溶液后,Ca2+,Mg2+,Ba2…”相关的问题
更多“加入NaOH和Na2CO3溶液后,Ca2+,Mg2+,Ba2…”相关的问题
现有含NaOH和Na2CO3的样品1.1790g,用水溶解后以酚酞为指示剂,加c(HCl)=0.3000mol/L HCl溶液48.16mL时,溶液变为无色,再加甲基橙指示剂,继续用该酸滴定,则需消耗24.08mL,计算样品中NaOH和Na2CO3的含量。
滴定0.7050g含Na2C2O4·H2O和H2C2O4·2H2O及惰性物质的样品,消耗0.1070mol/L NaOH溶液34.40mL,滴定后将溶液蒸发至干,并灼烧至Na2CO3,残渣溶于水后,用50.00mL 0.1250mol/L HCl处理,中和过量的HCl消耗2.59mL NaOH溶液。计算样品中Na2C2O4·H2O和H2C2O4·2H2O的含量。
化合物A、B的分子式都是C4H6O2,它们都不溶于NaOH溶液,也不与Na2CO3作用,但可使溴水褪色,有类似乙酸乙酯香味。它们与NaOH共热后,A生成CH3COONa和CH3CHO,B生成甲醇和羧酸钠盐C,该钠盐用硫酸中和后蒸馏出的有机物D可使溴水褪色。写出A、B、C、D的结构简式及有关反应方程式。
含有NaOH和Na2CO3以及中性杂质的试样0.2000g,用0.1000mol·L-1HCl溶液22.20mL滴定至酚酞终点,继续用HCl滴定至甲基橙终点,又用去12.20mL,计算试样中NaOH和Na2CO3的质量分数。
用0.1224mol/L HCl滴定可能含有NaOH、Na2CO3、NaHCO3的溶液,滴至酚酞终点消耗34.66mL。若滴至溴甲酚绿终点,消耗41.24mL,判断溶液的组成,并计算各组分的质量。
称取石灰石样品0.3000g,加入25.00mL HCl标准溶液,煮沸除去CO2后,用c(NaOH)=0.2000mol/L的NaOH溶液回滴,用去NaOH 5.84mL。求样品中CaCO3的质量分数,若折算成CaO,其质量分数又是多少?已知该HCl溶液20.00mL恰好与25.00mL的NaOH溶液完全反应。已知CaCO3、CaO的摩尔质量分别为100.09g/mol、56.08g/mol。
A.V1=V2
B.V1=2V2
C.2V1=V2
D.V1>V2
E.V1<V2
测定氮肥中NH3的含量。称取试样1.6160g,溶解后在250mL容量瓶中定容,移取25.00mL,加入过量NaOH溶液,将产生的NH3导入40.00mLc(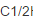 H2SO4)=0.1020mol/L的H2SO4标准溶液中吸收,剩余的H2SO4需17.00mLc(NaOH)=0.09600mol/L的NaOH溶液中和。计算氮肥中NH3的质量分数。
H2SO4)=0.1020mol/L的H2SO4标准溶液中吸收,剩余的H2SO4需17.00mLc(NaOH)=0.09600mol/L的NaOH溶液中和。计算氮肥中NH3的质量分数。
A.将Na2S2O3溶液煮沸1h,过滤,冷却后再标定
B.将Na2S2O3溶液煮沸1h,放置7天,过滤后再标定
C.用煮沸冷却后的纯水配制Na2S2O3溶液后,即可标定
D.用煮沸冷却后的纯水配制,放置7天后再标定
E.用煮沸冷却后的纯水配制,且加入少量Na2CO3,放置7天后再标定