 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
可逆反应在此温度下当A的解离度为50%时,反应在密闭容器中达到化学平衡,此时系统的总压力p为()
A.#图片1$#
B.#图片2$#
C.#图片3$#
D.#图片4$#
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.#图片1$#
B.#图片2$#
C.#图片3$#
D.#图片4$#
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“可逆反应在此温度下当A的解离度为50%时,反应在密闭容器中达…”相关的问题
更多“可逆反应在此温度下当A的解离度为50%时,反应在密闭容器中达…”相关的问题
 ,
, =-180kJ·mol-1,对此反应的逆反应来说,下列说法中正确的是( )
=-180kJ·mol-1,对此反应的逆反应来说,下列说法中正确的是( )A.升高温度,

C.增大压力,平衡移动 D.N2浓度增加,NO解离度增加
已知25℃时,Ka(HAc)=1.75×10-5。计算该温度下0.10mol·L-1HAc溶液中H+浓度及溶液的pH,并计算该浓度下HAc的解离度。
已知反应 的标准摩尔焓变
的标准摩尔焓变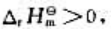 ,在一定温度下达到平衡状态。欲使N2O4的解离度增大,可采取的措施是()。
,在一定温度下达到平衡状态。欲使N2O4的解离度增大,可采取的措施是()。
A、将系统的体积压缩为原来的1/2
B、体积保持不变,加入惰性气体使压力增大到原来的2倍
C、压力保持不变,加入惰性气体使体积增大到原来的2倍
D、体积保持不变,加入NO气体使压力增大到原来的2倍
已知环己烷(1)-苯(2)系统在40℃时的活度系数模型为GE=0.458RTx1x2,纯组分的蒸气压为p
A.B为固态,Z为气态
B.B和Z均为气态
C.B和Z均为固态
D.B为气态,Z为固态
任何可逆反应在一定温度下,不论参加反应的物质的起始浓度如何,反应达到平衡时,各物质的平衡浓度相同。( )