 更多“温度为T K时,1 L pH=6的纯水中含10-6NA个OH…”相关的问题
更多“温度为T K时,1 L pH=6的纯水中含10-6NA个OH…”相关的问题
A.常温下pH=10的某碱溶液,取1 mL稀释到100 mL,稀释后pH为a,则a≥12
B.某温度下纯水中c(OH-)=2×10–7 mol·L-1,则该温度下0.1 mol·L–1的盐酸的pH=1
C.常温下pH=3的 H2SO4与pH=11的氨水等体积混合后,加入酚酞溶液仍为无色
D.用等浓度的NaOH溶液中和等体积pH=2与pH=3的醋酸,所消耗的NaO溶液的体积前者是后者的10倍
A.温度每增加10~15℃,微生物活动能力增加一倍
B.当pH<6.5或ph>9时,微生物生长受到抑制
C.水中溶解氧应维持2mg/l以上
D.微生物对氮、磷的需要量为BOD5:N:P=200:5:1(P210 比例应为100:5:1)
A.蒸馏水中,c(H+)•c(OH-)=1×10-14
B.纯水中,25 ℃时,c(H+)•c(OH-)=1×10-14
C.25 ℃时,任何以水为溶剂的稀电解质溶液中,c(H+)•c(OH-)=1×10-14
D.KW值随温度升高而增大
为防止热量损失而绝缘起来的一根棒,一端浸在100℃的沸水中,另一端浸在冰水混合物中。棒由长1.00m的铜(其一端在沸水中)和长为L的钢(其一端在冰水中)组成,两棒的截面积均为5.00cm2,达到稳态时,两者的接头处温度为60℃。已知铜、钢的热导率分别为385W/(m·K)和50.2W/(m·K)。求:
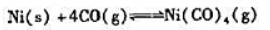
(1)不查附表,判断该反应是嫡增反应还是煽减反应.
(2)在某温度下该反应自发进行,推测反应自发进行时环境的璃是增加还是减少.
(3)利用附表一中所查到的数据,计算25℃下该反应的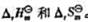
(4)当该反应的时,温度为多少?
(5)在提纯镍的Mond过程中,第一步是粗镍与CO,Ni(CO)4(四羰基合镍)在50℃左右的温度下达到平衡,这一步的标准平衡常数应尽可能的大,以便使镍充分地变成气相化合物.计算50℃下上述反应的标准平衡常数Kθ.
(6)在Mond过程中的第二步,将气体混合物从反应器中除去,并将其加热至230℃左右.在足够高的温度下的正、负号可以转换,反应在相反方向上发生,沉积出纯镍.在这一步,前述反应的标准平衡常数应尽可能的小.计算在230℃下该反应的标准平衡常数.
(7)Mond过程的成功依赖于Ni(CO)4的挥发性.在室温条件下,Ni(CO)4是液体,42.2℃时沸腾,其汽化焓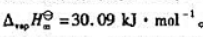 计算该化合物的汽化熵
计算该化合物的汽化熵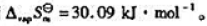
(8)近来改进了的Mond过程是在较高压力和150℃下进行第一步反应的.估算150℃下,Ni(CO)4,将要液化之前所能达到的最大压力(即估算150℃下,Ni(CO)4(l)的蒸气压).
设X=C[0,1],k为闭单位正方形
S={(s,t):0≤s,t≤1)
上的纯量连续函数。设A:X→X定义为
![设X=C[0,1],k为闭单位正方形 S={(s,t):0≤s,t≤1) 上的纯量连续函数。设A](https://img2.soutiyun.com/latex/latex.action)
求证:A为紧算子。
A.钙离子:在pH12~13时,以钙-羧酸为指示剂,用EDTA标准溶液滴定溶液由紫红色变为亮蓝色为终点
B.钙镁总量:在pH=10时,以铬黑T为指示剂,用EDTA标溶液滴定至溶液由紫红色变为纯蓝色为终点
C.测定的钙镁总量减去钙的量即为镁的量
D.测定中加入三乙醇胺用于消除铁、铝的干扰
E.用NH3-NH4Cl缓冲溶液调节溶液pH=10
某1、2两组分构成二兀系,活度系数方程为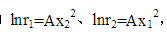 ,端值常数与温度的关系:A=1.7884-4.25×10-3T(T,K)
,端值常数与温度的关系:A=1.7884-4.25×10-3T(T,K)
蒸气压方程为:
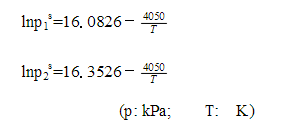 假设汽相是理想气体,试问99.75kPa时(1)系统是否形成恒沸物?(2)恒沸温度是多少?
假设汽相是理想气体,试问99.75kPa时(1)系统是否形成恒沸物?(2)恒沸温度是多少?
一个温度计插入100℃的水中测温,经3min后指示95℃,如果温度计可视为一个一阶环节,且K=1,求:
(1)时间常数T;
(2)其数学模型;
(3) T=1min时,温度计的指示值是多少?


 如果结果不匹配,请
如果结果不匹配,请 

















