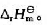题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知NO(g)和NO2(g)的分别为90.3kJ·mol-1和33.2kJ·mol-1,反应NO2(g)→NO(g)+1/2O2(g)的为()。 (A) 33.2kJ·m
已知NO(g)和NO2(g)的

(A) 33.2kJ·mol-1(B) 57.1kJ·mol-1
(C) 123.5kJ·mol-1(D) 90.3kJ·mol-1
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知NO(g)和NO2(g)的

(A) 33.2kJ·mol-1(B) 57.1kJ·mol-1
(C) 123.5kJ·mol-1(D) 90.3kJ·mol-1
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知NO(g)和NO2(g)的分别为90.3kJ·mol-1…”相关的问题
更多“已知NO(g)和NO2(g)的分别为90.3kJ·mol-1…”相关的问题
298 K时,反应N2O4(g)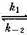 2NO2(g)的速率常数
2NO2(g)的速率常数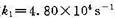 ,已知N2O4(g)和NO2(g)的标准摩尔生成Gibbs自由能分别为
,已知N2O4(g)和NO2(g)的标准摩尔生成Gibbs自由能分别为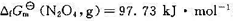 和
和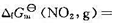 51.25 kJ·mol-1。请计算:(1)在298 K时,N2O4(g)的初始压力为100 kPa,NO2(g)的平衡分压;(2)该反应的弛豫时间r。
51.25 kJ·mol-1。请计算:(1)在298 K时,N2O4(g)的初始压力为100 kPa,NO2(g)的平衡分压;(2)该反应的弛豫时间r。
体积为1dm3的抽空密闭容器中放有0.03458molN2O4(g),发生如下分解反应:

50℃时分解反应的平衡总压为130.0kPa.已知25℃时N2O4(g)和NO2(g)的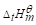
分别为9.16kJ·mol-1和33.18kJ·mol-1.设反应的ΔTGp,m=0.
(1)计算50℃时N2O4(g)的解离度及分解反应的Kθ;
(2)计算100C时反应的Kθ.
有双分子反应CO(g)+NO2(g)→CO2(g)+NO(g), e知在540~727 K之间发生定容反应,其速率常数k的表达式为
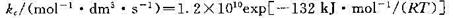
若在600 K时,CO(g )和NO2(g)的初始压力分别为667 Pa和933 Pa.试计算:(1)该反应在600 K时的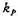 值;(2)反应进行10h后,NO的分压。
值;(2)反应进行10h后,NO的分压。
已知液体甲苯(A)和液体苯(B)车90℃对的施和蒸气分别为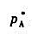 =54.22kPa和
=54.22kPa和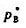 =136.12kPa;两者可形成理想液态琵混合物.今有系统组成为xB,o=0.3的甲苯-苯混合物5mol,在90℃下成气-液两相平衡,若气相组成为ya=0.4556,求:
=136.12kPa;两者可形成理想液态琵混合物.今有系统组成为xB,o=0.3的甲苯-苯混合物5mol,在90℃下成气-液两相平衡,若气相组成为ya=0.4556,求:
(1)平衡时液相组成xB及系统的压力p;
(2)平衡时气.液两相的物质的量n(g),n(l)
有基元反应Cl(g)+H2(g)→HCl(g)+H(g),已知它们的摩尔质量和直径分别为
MCl=35.45g·mol-1,-1=2.016g·mol-1
dCl=0.20nm,
已知CH3COOH(g),CH4(g)和CO2(g)的平均摩尔定压热容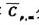 分别为52.3J·mol-1·K-1,37.7J·mol-1·K-1和31.4J·mol-1·K-1.试由教材附录中三化合物的标准摩尔生成焓计算1000K时下列反应的
分别为52.3J·mol-1·K-1,37.7J·mol-1·K-1和31.4J·mol-1·K-1.试由教材附录中三化合物的标准摩尔生成焓计算1000K时下列反应的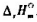 .
.
A.N(NO2)3分子是平面三角形
B.分子中四个氮原子共平面
C.该分子中的中心氮原子还有一对孤电子对
D.15.2 g该物质含有6.02×1022个原子
1
·K-1,37.7J·mol-1·K-1和31.4J·mol-1·K-1试由附录中三化合物的标准摩尔生成焓计算1000K时下列反应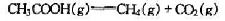 的
的