 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用同一浓度的高锰酸钾溶液滴定体积相等的FeSO4和Na2C204,假若消耗溶液体积相同,那么浓度(mol/L)关系为()。
A.[FeS04]=2[Na2C2O4]
B.[FeSO4]=[NaC2O4]
C.2[FeS04]=[Na2C2O4]
D.[FeSO4]=4[Na2C2O4]
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.[FeS04]=2[Na2C2O4]
B.[FeSO4]=[NaC2O4]
C.2[FeS04]=[Na2C2O4]
D.[FeSO4]=4[Na2C2O4]
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“用同一浓度的高锰酸钾溶液滴定体积相等的FeSO4和Na2C2…”相关的问题
更多“用同一浓度的高锰酸钾溶液滴定体积相等的FeSO4和Na2C2…”相关的问题
A.c(FeSO4)=2c(H2C2O4)
B.c(H2C2O4)=2c(FeSO4)
C.c(FeSO4)=c(H2C2O4)
D.c(FeSO4)=4c(H2C2O4)
用同一浓度的H2C2O4标准溶液,分别滴定等体积的KMnO4和NaOH两种溶液,化学计量点时如果消耗的标准溶液体积相等,说明NaOH溶液的浓度是KMnO4溶液浓度的5倍。( )
A.#图片0$#
B.#图片1$#
C.#图片2$#
D.#图片3$#
A.c(H2SO4)=c(HAc)
B.c(H2SO4)=2c(HAc)
C.2c(H2SO4)=c(HAc)
D.4c(H2SO4)=4c(HAc)
E.c(H2SO4)=4c(HAc)
A.氢离子浓度(单位:mol/L,下同)相等
B.H2SO4和HAc的浓度相等
C.H2SO4的浓度为HAc的浓度的1/2
D.H2SO4和HAc的电离度相等
A.c(FeSO4)=c(H2C2O4)
B.c(FeSO4)=2c(H2C2O4)
C.2c(FeSO4)=c(H2C2O4)
D.c(FeSO4)=4c(H2C2O4)
E.c(FeSO4)=6c(H2C2O4)
A.H2SO4溶液和HAc溶液中的氢离子浓度相等
B.H2SO4溶液的氢离子浓度是HAc溶液的氢离子浓度的2倍
C.H2SO4溶液的浓度与HAc溶液的浓度相等
D.H2SO4溶液的浓度是HAc溶液的浓度的1/2
A.V1=V2
B.V1>V2
C.V1<V2
D.V1=2V2
E.V2=2V1
用CLa(No3)3=0.03318mol?L-1的La(NO3)3溶液滴定100.0mL 0.03095mol?L-1的NaF的溶液,滴定反应为:
 ,用固体LaF。膜电极为指示电极(正极),饱和甘汞电极为参比电极(负级),测得其滴定数据为:
,用固体LaF。膜电极为指示电极(正极),饱和甘汞电极为参比电极(负级),测得其滴定数据为:
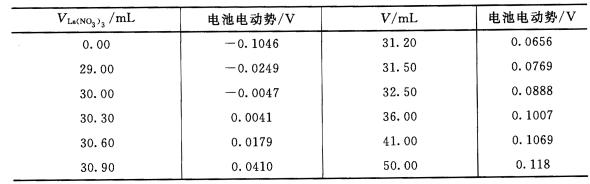 (1)计算反应完全时所需滴定剂的体积,并将其与电位滴定确定终点时消耗滴定剂的体积相比较。 (2)已知电池电动势与F一浓度的关系为:E=K+0.0592PF,用所测第一组数据算出K值。 (3)用求得的K值,计算加入50.00mI.,滴定剂后r的浓度?(设活度系数不变)
(1)计算反应完全时所需滴定剂的体积,并将其与电位滴定确定终点时消耗滴定剂的体积相比较。 (2)已知电池电动势与F一浓度的关系为:E=K+0.0592PF,用所测第一组数据算出K值。 (3)用求得的K值,计算加入50.00mI.,滴定剂后r的浓度?(设活度系数不变)
用0.1000mol·L-1NaOH溶液滴定50.00mL一元弱酸的数据如下:
(a)绘制滴定曲线;
(b)绘制 曲线;
曲线;
(c)用二级微商法确定终点;
(d)计算试样中弱酸的浓度;
(e)化学计量点的PH应为多少?
(f)计算此弱酸的电离常数(提示:根据滴定曲线上的半中和点的PH)。
| 体积/mL | pH |
| 0.00 1.00 2.00 4.00 7.00 10.00 12.00 14.00 15.00 15.50 15.60 15.70 15.80 16.00 17.00 20.00 24.00 28.00 | 3.40 4.00 4.50 5.05 5.47 5.85 6.11 6.60 7.04 7.70 8.24 9.43 10.03 10.61 11.30 11.96 12.39 12.57 |