 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
称取5g混和均匀的试样,于100ml的锥形瓶中,加入()(1mol/L)的盐酸溶液
A.10ml
B.30ml
 答案
答案
B、30ml
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.10ml
B.30ml
 答案
答案
B、30ml
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“称取5g混和均匀的试样,于100ml的锥形瓶中,加入()(1…”相关的问题
更多“称取5g混和均匀的试样,于100ml的锥形瓶中,加入()(1…”相关的问题
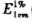 (245nm)=560]
(245nm)=560]
某钢样含镍约0.12%,用丁二酮肟光度法(ε=1.3×104L·mol-1·cm-1)进行测定。试样溶解后,转入100mL容量瓶中,显色,并加水稀释至刻度。取部分试液于波长470nm处用1cm吸收池进行测量。如要求此时的测量误差最小,应称取试样多少克?
为分析硅酸岩中铁、铝、钛的含量,称取试样0.6050g。除去SiO2后,用氨水沉淀铁、铝、钛为氢氧化物沉淀。沉淀灼烧为氧化物后的质量为0.4120g;再将沉淀用K2S2O7熔融,浸取液定容于100mL容量瓶,移取25.00mL试液通过锌汞还原器,此时Fe3+还原为Fe2+,Ti4+还原为Ti3+,还原液流入Fe3+溶液中,滴定时消耗了0.01388mol/L K2Cr2O710.05mL;另移取25.00mL试液用SnCl2还原Fe3+后,再用上述K2Cr2O7溶液滴定,消耗了8.02mL。计算试样中Fe2O3、Al2O3、TiO2的质量分数。
称取Sb2S3试样1.2647g,将其在氧气流中灼烧所产生的SO2气体通入100mL FeCl3溶液中,使Fe3+还原至Fe2+,取该溶液10mL,用c(
比色皿测量,希望此时测量误差最小,应称取试样多少克?已知摩尔吸光系数为1.3×104L·mol-1·cm-1。