 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
1mol水蒸气(H2O,g)在100℃,101.325kPa下全部凝结成液态水。求过程的功。
1mol水蒸气(H2O,g)在100℃,101.325kPa下全部凝结成液态水。求过程的功。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
1mol水蒸气(H2O,g)在100℃,101.325kPa下全部凝结成液态水。求过程的功。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“1mol水蒸气(H2O,g)在100℃,101.325kPa…”相关的问题
更多“1mol水蒸气(H2O,g)在100℃,101.325kPa…”相关的问题
SƟH2O(g)>(298K)= 188.72J/(K·mol)。
1mol水H2O(1)在恒压下自O℃经不同的升温方式被加热至100℃,求水、热源的熵变及总熵变。 (1)水与100℃的恒温热源接触升至100℃; (2)水先与50℃的恒温热源接触,达平衡后再与100℃的恒温热源接触升温至100℃; (3)用何种加热方式既能使水温升至100℃,又能使总熵变接近于零。 已知H2O(1)的摩尔恒压热容为75.40J.K-1.mol-1。
已知水(H2O,I)在100℃的饱和蒸气压p=101.325kPa,在此温度.压力下水的摩尔蒸发焓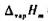 =40.668kJ·mol-1.求在100℃,101.325kPa下使1kg水蒸气全部凝结成液体水时的Q,W,ΔU和ΔH.设水蒸气适用理想气体状态方程.
=40.668kJ·mol-1.求在100℃,101.325kPa下使1kg水蒸气全部凝结成液体水时的Q,W,ΔU和ΔH.设水蒸气适用理想气体状态方程.
100℃时在一个体积恒定为5.0m3的真空容器中有一装有lmol水H2O(1)的小玻璃泡,若将玻璃泡打碎,求此过程的热。已知H2O(1)在正常沸点时的摩尔蒸发焓为40.66kJ.mol-1。设水蒸气可作为理想气体。
已知 CO2(g) NH3(g) H2O(g) CO(NH2)2(s)


通过计算说明,反应CO2(g)+2NH3(g)===H2O(g)+CO(NH2)2(s)
(1)在298K时,反应能否正向自发进行?
(2)在1000K时,反应能否正向自发进行?
100℃的恒温槽中有一带活塞的圆筒,筒中有2mol的N2(g)及装于小玻璃瓶中的3mol的H2O(l)。环境的压力即系统的压力维持120kPa不变。今将小玻璃瓶打破,液体水蒸发到平衡态,求此过程的Q,W,△U,△H,△S,△A及△G。
已知:水在100℃时的饱和蒸气压ps=101.325kPa,在此条件下水的摩尔蒸发焓△vapHm=40.668J·mol-1。
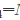 Na2SO4+S↓+SO2↑+H2O在室温下反应,以下4组溶液最先出现浑浊的是()
Na2SO4+S↓+SO2↑+H2O在室温下反应,以下4组溶液最先出现浑浊的是()A.0.1mol/LNa2S2O3和0.1mol/LH2SO4等体积混合
B.0.5 mol/LNa2S2O3和0.5mol/LH2SO4等体积混合
C.1mol/LNa2S2O3和1mol/LH2SO4等体积混合
D.0.5mol/LNa2S2O3和1mol/LH2SO4等体积混合