 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某反应的速率方程为r=kcA2,则指前因子的单位为()。A.kJ.mol-1B.s-1C.mol.L-1.s-1D.L.mol-1.s-
某反应的速率方程为r=kcA2,则指前因子的单位为()。
A.kJ.mol-1
B.s-1
C.mol.L-1.s-1
D.L.mol-1.s-1
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某反应的速率方程为r=kcA2,则指前因子的单位为()。
A.kJ.mol-1
B.s-1
C.mol.L-1.s-1
D.L.mol-1.s-1
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某反应的速率方程为r=kcA2,则指前因子的单位为()。A.…”相关的问题
更多“某反应的速率方程为r=kcA2,则指前因子的单位为()。A.…”相关的问题
某溶液的反应A+B→P,当A和B的起始浓度为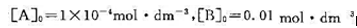 时,实验测得不同温度下吸光度随时间的变化如下表:
时,实验测得不同温度下吸光度随时间的变化如下表:
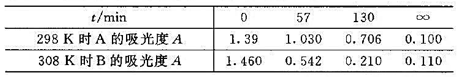
当固定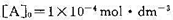 ,改变[B]o时,实验测得在298 K时,t1/2随[B]0的变化如下表:
,改变[B]o时,实验测得在298 K时,t1/2随[B]0的变化如下表:

设速率方程为r=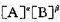 ,试计算α、β、速率常数k和实验活化能
,试计算α、β、速率常数k和实验活化能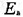 。
。
某气态物质A(g)在固体催化剂上发生异构化反应,其机理如下:
![某气态物质A(g)在固体催化剂上发生异构化反应,其机理如下:式中,[K]为催化剂的活性中心。设表面某](https://img2.soutiyun.com/ask/2020-04-29/957006854414219.png)
式中,[K]为催化剂的活性中心。设表面反应为决速步,假定催化剂表面是均匀的。(1)导出反应的速率方程;(2)在373 K时测得,高压下的速率常数k高压= 500 kPa·s-1,低压下的速率常数k低压=10s-1.求aA的值和该温度下,当反应速率r=![某气态物质A(g)在固体催化剂上发生异构化反应,其机理如下:式中,[K]为催化剂的活性中心。设表面某](https://img2.soutiyun.com/ask/2020-04-29/957006869364397.png) 时A(g)的分压。
时A(g)的分压。
A.r=kc(NO2)2
B.r=kc(NO2)c(CO)
C.r=kc2(NO2)c(CO)
D.r=kc(CO)
Lindemann 单分子反应理论认为,单分子反应的历程为
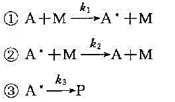
(1)请用推导证明,反应速率方程为r=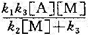 。
。
(2)请应用简单碰撞理论计算469℃时的k1,已知2-丁烯的d=0.5 nm,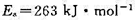 ;
;
(3)若反应速率方程写成r=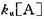 ,且
,且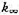 为高压极限时的表观速率常数,请计算
为高压极限时的表观速率常数,请计算 的压力P1/2,已知
的压力P1/2,已知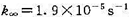 ;
;
(4)实验测得丁烯异构化在469℃时的p1/2=0.532 Pa,试比较理论计算的p1/2(理论)与实验值p1/2(实验)之间的差异,对此你有何评论?
一定温度下,对反应2A====B+D,实验测定了如下数据:
cA/(mol·L-1) 0.40 0.20
速率/(mol·L-1·min-1) 0.02 0.01
则该反应的速率方程为r=______,速率常数k=______。